Prostaatkanker: samenvatting
Prostaatkanker (PCa) blijft een belangrijke doodsoorzaak bij Amerikaanse mannen en de prevalentie blijft wereldwijd stijgen, vooral in landen waar mannen een 'westers' dieet volgen. Epidemiologische, preklinische en klinische studies suggereren een mogelijke rol voor inname via de voeding op de incidentie en progressie van PCa. 'Deze minireview geeft een overzicht van recent gepubliceerde literatuur met betrekking tot voedingsstoffen, voedingsfactoren, voedingspatronen en incidentie en progressie van PCa. Een lage inname van koolhydraten, soja-eiwit, omega-3 (w-3) vet, groene thee, tomaten en tomatenproducten en zyflamend bleken veelbelovend bij het verminderen van PCa-risico of -progressie. Een hogere inname van verzadigd vet en een hogere β-caroteenstatus kunnen het risico verhogen. Er kan een U-vormige relatie bestaan tussen foliumzuur, vitamine C, vitamine D en calcium met PCa-risico. Ondanks de inconsistente en onduidelijke bevindingen, is het potentieel voor een rol van inname via de voeding voor de preventie en behandeling van PCa veelbelovend. De combinatie van alle gunstige factoren voor PCa risicoreductie in een gezond voedingspatroon is misschien wel het beste voedingsadvies. Dit patroon omvat rijk fruit en groenten, minder geraffineerde koolhydraten, totale en verzadigde vetten en minder gekookt vlees. Verdere zorgvuldig opgezette prospectieve studies zijn gerechtvaardigd.
Trefwoorden: Dieet, Prostaatkanker, Voedingsstoffen, Voedingspatroon, Lifestyle, Preventie, Behandeling, Voeding, Dieetinterventie, Review
Inhoud
Inleiding: Prostaatkanker
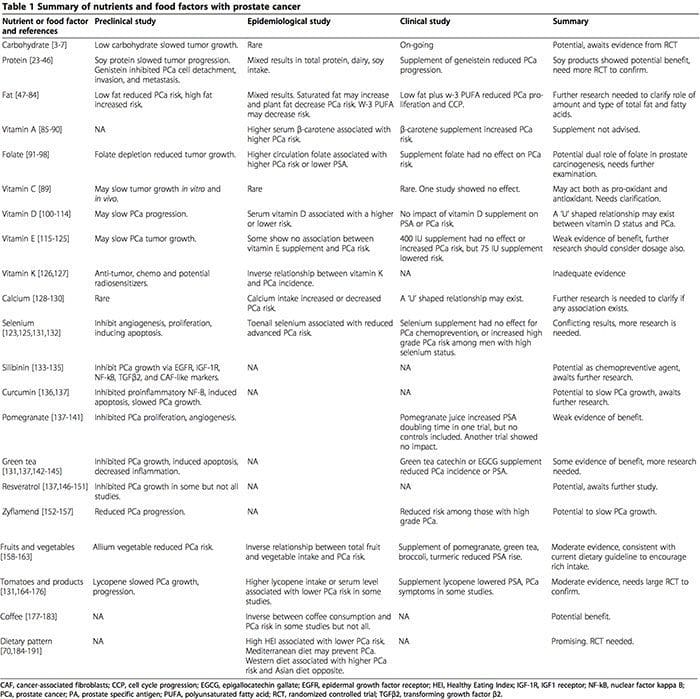
Prostaatkanker (PCa) is de tweede meest voorkomende vorm van kanker bij mannen, met bijna een miljoen nieuwe gevallen per jaar wereldwijd [1], met een ongeveer zes keer hogere incidentie in westerse dan in niet-westerse landen. Aangenomen wordt dat voeding, levensstijl, omgevingsfactoren en genetische factoren een rol spelen bij deze verschillen. Deze beoordeling richt zich op het meest recente bewijs van de mogelijke rol van voedingsfactoren op PCa en omvat epidemiologisch en klinisch onderzoek voor de impact van eiwitten, vetten, koolhydraten, vezels, fytochemicaliën, andere voedselcomponenten, volwaardige voedingsmiddelen en voedingspatronen op de incidentie, ontwikkeling en/of progressie van PCa. Gegevens uit meta-analyses of goed opgezette gerandomiseerde onderzoeken en prospectieve studies worden in dit overzicht benadrukt. Opgemerkt moet worden dat studies naar inname via de voeding of voeding en kanker vaak onderhevig zijn aan verschillende beperkingen en dus de interpretatie van de resultaten bemoeilijken. Wanneer bijvoorbeeld een onderzoek is opgezet om het effect van de hoeveelheid vetinname te onderzoeken, zal een verandering in de vetinname onvermijdelijk de inname van eiwitten en/of koolhydraten veranderen, en mogelijk ook de inname van andere voedingsstoffen. Als gevolg hiervan is het moeilijk om het effect alleen toe te schrijven aan een verandering in de vetinname. Bovendien omvat de impact van macronutriënten mogelijk aspecten van zowel de absolute hoeveelheid als het type geconsumeerde macronutriënten. Beide aspecten kunnen onafhankelijk van elkaar het ontstaan en/of de ontwikkeling van kanker beïnvloeden, maar zijn niet altijd van elkaar te onderscheiden in onderzoeksontwerpen. Hoewel dit onderwerp onlangs is herzien [2], wordt, gezien de uitgebreide nieuwe literatuur over het onderwerp, hierin een bijgewerkt overzicht gepresenteerd en wordt een samenvattende tabel gegeven voor een snelle referentie (Tabel 1).
Voedingsstoffen Koolhydraten Gezien de hypothese dat insuline een groeifactor is voor PCa, is de hypothese dat het verminderen van koolhydraten en dus het verlagen van seruminsuline de PCa-groei kan vertragen [3]. Inderdaad, in diermodellen heeft een koolhydraatarm ketogeen dieet (NCKD) [4,5] of een koolhydraatarm dieet (20% kcal als koolhydraat) gunstige effecten op het vertragen van de groei van prostaattumoren [6,7]. In studies bij mensen bleek uit één studie dat een hoge inname van geraffineerde koolhydraten geassocieerd was met een verhoogd risico op PCa [7]. Naast de hoeveelheid koolhydraten kan het type koolhydraten van invloed zijn op PCa, maar onderzoek heeft geen uitsluitsel gegeven. Het potentieel om het risico en de progressie van PCa te verminderen door het koolhydraatmetabolisme te beïnvloeden, wordt actief onderzocht met Metformine. Metformine verminderde proliferatie van PCa-cellen en vertraagde progressie in respectievelijk vitro en in vivo [8-10] en verminderde incidentrisico en mortaliteit bij mensen [11-13]. Twee klinische onderzoeken met één arm toonden ook een positief effect van metformine bij het beïnvloeden van markers van proliferatie en progressie van PCa [14,15]. Andere retrospectieve cohortstudies hebben echter geen effect van metformine op recidief- of incidentrisico van PCa ondersteund [16-22]. Ondanks het potentieel voor het verminderen van totale of enkelvoudige koolhydraten ten gunste van PCa-controle, ontbreekt bewijs uit gerandomiseerde gecontroleerde onderzoeken (RCT). Er lopen momenteel twee gerandomiseerde onderzoeken naar de impact van een koolhydraatarm dieet (ongeveer 5% kcal) op de PSA-verdubbelingstijd bij PCa-patiënten na radicale prostatectomie (NCT01763944) en op de glykemische respons bij patiënten die starten met androgeendeprivatietherapie (ADT) ( NCT00932672). Bevindingen van deze onderzoeken zullen licht werpen op het effect van koolhydraatinname op markers van PCa-progressie en de rol van verminderde koolhydraatinname bij het compenseren van de bijwerkingen van ADT.
Eiwit
Het ideale niveau van eiwitinname voor een optimale algehele gezondheid of prostaatgezondheid is onduidelijk. Ondanks de populariteit van koolhydraatarme diëten met een hoog eiwitgehalte, meldden recente studies bij mensen dat een lage eiwitinname geassocieerd was met een lager risico op kanker en algehele mortaliteit bij mannen van 65 jaar en jonger. Onder mannen ouder dan 65 jaar was een lage eiwitinname geassocieerd met een hoger risico op kanker en algehele mortaliteit [23]. In diermodellen had de verhouding tussen eiwitten en koolhydraten invloed op de cardiometabole gezondheid, veroudering en levensduur [24]. De rol van voedingseiwitten en de eiwit-koolhydraatverhouding op de ontwikkeling en progressie van PCa vereist nader onderzoek.
Dierlijke Eiwitten
Het bestuderen van de eiwitinname kan, net als alle aspecten van de voedingswetenschap, een uitdaging zijn. Zo bestaat dierlijk vlees, een bron van eiwitten in westerse diëten, niet alleen uit eiwitten, maar ook uit vet, cholesterol, mineralen en andere voedingsstoffen. De hoeveelheid van deze voedingsstoffen, inclusief vetzuren, kan variëren van dierlijk vlees tot dierlijk vlees. Eerdere studies bij mensen hebben aangetoond dat de consumptie van gevogelte zonder vel, dat minder cholesterol en minder verzadigd vet bevat dan veel rood vlees, niet geassocieerd was met het opnieuw optreden of de progressie van PCa [25]. De consumptie van gebakken gevogelte was echter omgekeerd geassocieerd met geavanceerde PCa [26,27], terwijl gekookt rood vlees geassocieerd was met een verhoogd risico op geavanceerde PCa [26,27]. De manier waarop het voedsel wordt bereid, kan dus de impact op het risico en de progressie van PCa wijzigen. Over het algemeen kan visconsumptie in verband worden gebracht met verminderde PCa-sterfte, maar op hoge temperatuur gekookte vis kan bijdragen aan PCa-carcinogenese [28]. Het kan dus raadzaam zijn om regelmatig vis te consumeren, maar de kooktemperatuur moet gematigd worden gehouden.
Op zuivel gebaseerde eiwitten
Een andere veel voorkomende eiwitbron zijn zuivelproducten, zoals melk, kaas en yoghurt. Eerdere studies hebben aangetoond dat zuivel het algehele PCa-risico verhoogde, maar niet met agressieve of dodelijke PCa [29,30]. Bovendien werd gemeld dat zowel de consumptie van volle melk als de consumptie van magere melk PCa-progressie bevordert of vertraagt [29,31]. In het follow-upcohort van Physicians Health met 21,660 mannen bleek de totale zuivelconsumptie geassocieerd te zijn met een verhoogde incidentie van PCa [32]. Met name vetarme of magere melk verhoogde het PCa-risico van lage kwaliteit, terwijl volle melk het fatale PCa-risico verhoogde. Hoewel de exacte component(en) van zuivelproducten die deze associaties veroorzaken onbekend is, kunnen de hoge concentraties verzadigd vet en calcium een rol spelen. Een cross-sectionele studie van 1798 mannen toonde aan dat zuiveleiwit positief geassocieerd was met serum IGF-1 [33] niveaus die de initiatie of progressie van PCa kunnen stimuleren. Er is dus verder onderzoek nodig om de relatie tussen zuivelinname en PCa te verduidelijken. Er zijn onvoldoende gegevens om aanbevelingen te doen die specifiek verband houden met het risico of de progressie van zuivel of zuiveleiwitten en PCa.
Plantaardige Eiwitten
Soja en producten op basis van soja zijn rijk aan eiwitten en fyto-oestrogenen die PCa-preventie kunnen vergemakkelijken, maar de rol ervan op PCa is onduidelijk. In een studie bij muizen werd de inname van sojaproducten in verband gebracht met verminderde hepatische aromatase, 5β-reductase, expressie van androgeenreceptor en zijn gereguleerde genen, FOXA1, gewicht van het urogenitale kanaal en PCa-tumorprogressie [34]. Een recent gerandomiseerd onderzoek onder 177 mannen met een risicovolle ziekte na radicale prostatectomie wees uit dat suppletie met soja-eiwitten gedurende twee jaar geen effect had op het risico op recidief PCa [35]. Hoewel epidemiologische en preklinische studies [36,37] een mogelijke rol voor soja-/soja-isoflavonen bij PCa-risicovermindering of -progressie ondersteunen, vond een meta-analyse geen significante invloed van soja-inname op PSA-waarden, geslachtshormoonbindend globuline, testosteron, vrij testosteron, oestradiol of dihydrotestosteron [38]. Een andere RCT bij patiënten vóór prostatectomie vond ook geen enkel effect van soja-isoflavonsupplement tot zes weken op PSA, serum totaal testosteron, vrij testosteron, totaal oestrogeen, oestradiol of totaal cholesterol [39]. Aangezien de meeste uitgevoerde RCT's klein en van korte duur zijn, is verder onderzoek nodig.
Veel onderzoeken zijn doorgegaan met het onderzoeken van het primaire isoflavon in soja, genisteïne, en het effect ervan op PCa. Het potentieel voor genisteïne om loslating, invasie en metastase van PCa-cellen te remmen, wordt gerapporteerd [40]. Genisteïne kan glucose-update en glucosetransporter (GLUT) -expressie in PCa-cellen wijzigen [41], of zijn antitumoreffect uitoefenen door verschillende microRNA's omlaag te reguleren [42]. Studies met behulp van tumorcellen en diermodellen suggereren dat genisteïne kan concurreren met endogene oestrogenen en deze kan blokkeren voor binding aan de oestrogeenreceptor, waardoor cellulaire proliferatie, groei en differentiatie wordt geremd en, in het bijzonder, kan genisteïne celloslating, proteaseproductie, celinvasie remmen en zo metastase voorkomen [36,40,43]. Noch plasma- noch urinaire genisteïnespiegels waren echter geassocieerd met PCa-risico in case-control studies [44,45]. In een fase 2 placebogecontroleerde RCT met 47 mannen verminderde suppletie van 30 mg genisteïne gedurende drie tot zes weken de androgeengerelateerde markers van PCa-progressie aanzienlijk [46]. Bovendien kan genisteïne gunstig zijn bij het verbeteren van cabazitaxel-chemotherapie bij gemetastaseerde castratieresistente PCa [37]. Klinische studies zijn gerechtvaardigd om de rol van soja en soja-isoflavonen voor PCa-preventie of -behandeling verder te onderzoeken. Een definitieve aanbeveling met betrekking tot eiwitinname voor PCa-preventie of -behandeling is nog niet beschikbaar.
Vet
Onderzoeksresultaten die vetconsumptie met PCa-risico of -progressie onderzoeken, zijn tegenstrijdig. Zowel de totale absolute inname [47] van voedingsvet als de relatieve vetzuursamenstelling kunnen onafhankelijk verband houden met PCa-initiatie en/of -progressie. Hoewel dierstudies herhaaldelijk aantonen dat het verminderen van de inname van vet via de voeding de tumorgroei vertraagt [48-50] en vetrijke diëten, met name dierlijk vet en maïsolie, de PCa-progressie verhogen [51], zijn gegevens bij de mens minder consistent. Case-controlstudies en cohortstudies hebben ofwel geen verband aangetoond tussen totale vetconsumptie en PCa-risico [52-55] ofwel een omgekeerd verband tussen vetinname en PCa-overleving, vooral bij mannen met gelokaliseerde PCa [47]. Bovendien toonde een cross-sectioneel onderzoek aan dat vetinname uitgedrukt als percentage van de totale calorie-inname positief geassocieerd was met PSA-waarden bij 13,594 mannen zonder PCa [56]. Gezien deze tegenstrijdige gegevens is het mogelijk dat het type vetzuur [56] in plaats van de totale hoeveelheid een belangrijke rol speelt bij de ontwikkeling en progressie van PCa. Een studie wees uit dat plasma-verzadigde vetzuren positief geassocieerd zijn met PCa-risico in een prospectief cohort van 14,514 mannen van de Melbourne Collaborative Cohort Study [57]. Bovendien bleek uit een andere studie dat het eten van meer plantaardig vet geassocieerd was met een verminderd PCa-risico [58]. Deze onderzoeken ondersteunen de huidige voedingsrichtlijn om minder dierlijk vet en meer plantaardig vet te eten.
De gegevens met betrekking tot de consumptie van omega-6 (w-6) en omega-3 (w-3) meervoudig onverzadigde vetzuren (PUFA) en het PCa-risico zijn ook tegenstrijdig. Hoewel er gegevens zijn die een verband ondersteunen tussen verhoogde w-6 PUFA-inname (voornamelijk afgeleid van maïsolie) en het risico op algehele en hoogwaardige PCa [57,59], ondersteunen niet alle gegevens een dergelijk verband [60]. Sterker nog, een grotere inname van meervoudig onverzadigd vet was geassocieerd met een lagere sterfte door alle oorzaken bij mannen met niet-gemetastaseerde PCa in de Health Professionals Follow-up studie [58]. Het gepostuleerde mechanisme dat w-6 PUFA's en PCa-risico met elkaar verbindt, is de omzetting van arachidonzuur (w-6 PUFA) in eicosanoïden (prostaglandine E-2, hydroxyeicosatetraeenzuren en epoxyeicosatrieenzuren) die leiden tot ontsteking en cellulaire groei [61]. Omgekeerd kunnen w-3 PUFA's, die voornamelijk worden aangetroffen in vette koudwatervissen, de groei van PCa vertragen via een aantal mechanismen [61-63]. In een onderzoek onder 48 mannen met PCa met een laag risico onder actief toezicht, toonde herhaalde biopsie in zes maanden aan dat prostaatweefsel w-3-vetzuren, vooral eicosapentaeenzuur (EPA), bescherming kunnen bieden tegen PCa-progressie [64]. In vitro- en dierstudies suggereren dat w-3 PUFA's ontstekingsremmende, pro-apoptotische, antiproliferatieve en anti-angiogene routes induceren [65,66]. Bovendien ontdekte een muisstudie waarin verschillende soorten vet werden vergeleken, dat alleen het visoliedieet (dat wil zeggen een op omega-3 gebaseerd dieet) de PCa-groei vertraagde in vergelijking met andere voedingsvetten [67]. Met betrekking tot menselijke gegevens toonde een gerandomiseerde fase II-studie aan dat een vetarm dieet met w-3-suppletie vier tot zes weken voorafgaand aan radicale prostatectomie de proliferatie van PCa en de CCP-score (celcyclusprogressie) verminderde [62,68]. Een vetarm visoliedieet resulteerde in verlaagde 15(S)-hydroxyeicosatetraeenzuurspiegels en verlaagde CCP-score in vergelijking met een westers dieet [69]. De potentiële voordelen van omega-3-vetzuren uit vis worden ondersteund door epidemiologische literatuur die aantoont dat de inname van w-3-vetzuren omgekeerd geassocieerd was met fataal PCa-risico [70,71]. Ondanks de belofte van omega-3-vetzuren zijn niet alle onderzoeken het daarmee eens. Suppletie van 2 g alfa-linoleenzuur (ALA) per dag gedurende 40 maanden bij 1,622 mannen met PSA <4 ng/ml veranderde hun PSA niet [72]. Uit een andere studie bleek echter dat een hoog serum n-3 PUFA en docosapentaeenzuur (DPA) geassocieerd was met een verlaagd totaal PCa-risico, terwijl een hoog serum EPA en docosahexaeenzuur (DHA) mogelijk geassocieerd was met een verhoogd hoogwaardig PCa-risico [73] . Verder onderzoek is nodig om de rol van omega-3 PUFA's bij de preventie of behandeling van PCa beter te begrijpen.
cholesterol
Veel preklinische onderzoeken hebben aangetoond dat de ophoping van cholesterol bijdraagt aan de progressie van PCa [74-76]. Er werd gesuggereerd dat een hoog cholesterolgehalte in Lin et al. BMC Medicine (2015) 13:3 Pagina 5 van 15 kan een risicofactor zijn voor solide tumoren, voornamelijk door de opwaartse regulatie van cholesterolsynthese, ontstekingsroutes [77] en intratumorale steroïdogenese [78]. Volgens een recente studie met 2,408 mannen gepland voor biopsie, was serumcholesterol onafhankelijk geassocieerd met de voorspelling van PCa-risico [79]. In overeenstemming met de cholesterolbevindingen, was het gebruik van het cholesterolverlagende medicijn statine na radicale prostatectomie (RP) significant geassocieerd met een verminderd risico op biochemisch recidief bij 1,146 radicale prostatectomiepatiënten [80]. Een andere studie toonde ook aan dat statines het PCa-risico kunnen verminderen door de progressie te verlagen [81]. Hoewel het mechanisme niet is vastgesteld, toonden recentere onderzoeken ook aan dat een laag high-density lipoprotein (HDL)-cholesterolgehalte geassocieerd was met een hoger risico op PCa en dat een hogere HDL dus beschermend was [81-84]. Deze bevindingen ondersteunen het idee dat een hart-gezonde voedingsinterventie die cholesterol verlaagt, ook de gezondheid van de prostaat ten goede kan komen.
Vitaminen en mineralen
Hierin zullen we de recente gegevens over vitamine A, B-complex, C, D, E en K en selenium bekijken. In de twee grote klinische studies: de Carotene and Retinol Efficacy Trial (CARET; PCa was een secundair resultaat) en de Diet and Health prospectieve cohortstudie van de National Institutes of Health-American Association of Retired Persons (NIH-AARP), werd overmatige suppletie met multivitaminen geassocieerd met een hoger risico op het ontwikkelen van agressieve PCa, vooral bij degenen die individuele β-caroteensupplementen gebruiken [85,86]. Evenzo werden hoge serum-β-caroteenspiegels geassocieerd met een hoger risico op PCa bij 997 Finse mannen in het Kuopio Ischemic Heart Disease Risk Factor-cohort [87]. Het β-caroteensupplement bleek echter geen invloed te hebben op het risico op dodelijke PCa tijdens de therapie [88], of in de Deense prospectieve cohortstudie van 26,856 mannen [89]. Circulerend retinol was ook niet geassocieerd met PCa-risico in een grote case-control studie [90]. Het verband tussen vitamine A en PCa is dus nog onduidelijk.
Preklinisch bewijs suggereert dat folaatdepletie de tumorgroei kan vertragen, terwijl suppletie geen effect heeft op groei of progressie, maar direct kan leiden tot epigenetische veranderingen via toename van DNA-methylatie [91]. Twee meta-analyses toonden ook aan dat circulerende foliumzuurspiegels positief geassocieerd waren met een verhoogd risico op PCa [92,93], terwijl folaat in de voeding of supplementair geen effect had op het PCa-risico [94] in een cohortstudie met 58,279 mannen in Nederland [ 95] en een case-control studie in Italië en Zwitserland [96]. Een studie van een cohort mannen die een radicale prostatectomie ondergingen bij verschillende Veterans Administration-faciliteiten in de VS, toonde zelfs aan dat hogere folaatspiegels in het serum geassocieerd waren met een lagere PSA en dus een lager risico op biochemisch falen [97]. Een andere studie met gegevens van de National Health and Health van 2007 tot 2010 Voeding Onderzoeksenquête toonde aan dat een hogere foliumzuurstatus beschermend kan zijn tegen verhoogde PSA-waarden bij 3,293 mannen van 40 jaar en ouder, zonder gediagnosticeerde PCa [98]. Er werd gesuggereerd dat folaat een dubbele rol kan spelen bij prostaatcarcinogenese en daarom wacht de complexe relatie tussen folaat en PCa op verder onderzoek [99].
Ondanks de potentiële rol van vitamine C (ascorbinezuur) als antioxidant bij antikankertherapie, zijn er weinig onderzoeken naar de inname via de voeding of suppletie van vitamine C. Een RCT toonde geen effect van vitamine C-inname op PCa-risico [89]. Bovendien kan vitamine C in hoge doses meer als een pro-oxidant werken dan als een antioxidant, wat het ontwerp en de interpretatie van het onderzoek bemoeilijkt.
De primaire actieve vorm van vitamine D, 1,25 dihydroxyvitamine D3 (calcitriol), helpt bij een goede botvorming, induceert differentiatie van sommige immuuncellen en remt pro-tumorroutes, zoals proliferatie en angiogenese, en er is gesuggereerd dat het het PCa-risico ten goede komt [100]; bevindingen blijven echter onduidelijk. Meer recente studies hebben aangetoond dat verhoogde vitamine D-spiegels in het serum geassocieerd waren met een verminderd PCa-risico [101,102]. Verder kan het aanvullen van vitamine D de PCa-progressie vertragen of apoptose in PCa-cellen induceren [103-105]. Andere studies rapporteerden echter geen effect van vitamine D-supplement op PSA [106] of geen effect van vitamine D-status op PCa-risico [107,108]. Sommige onderzoeken rapporteerden daarentegen dat een lagere vitamine D-status geassocieerd was met een lager PCa-risico bij oudere mannen [109], of een hogere serum-vitamine D geassocieerd was met een hoger PCa-risico [110,111]. Een studie suggereerde zelfs dat er mogelijk een U-vormige relatie bestaat tussen de vitamine D-status en PCa en dat het optimale bereik van circulerende vitamine D voor PCa-preventie smal kan zijn [112]. Dit komt overeen met de bevindingen voor andere voedingsstoffen dat een grotere inname van een gunstige voedingsstof niet altijd beter hoeft te zijn.
Een recent onderzoek toonde aan dat de associatie tussen vitamine D en PCa werd gemoduleerd door vitamine D-bindend eiwit [113], wat de eerdere inconsistente bevindingen mogelijk gedeeltelijk heeft verklaard. Verder rapporteerde een meta-analyse die de associatie tussen vitamine D-receptor (VDR) polymorfismen (BsmI en FokI) en PCa-risico onderzocht, geen relatie met PCa-risico [114]. De rol van vitamine D in PCa blijft dus onduidelijk.
In een groot gerandomiseerd onderzoek met in totaal 14,641 Amerikaanse mannelijke artsen van 50 jaar oud, kregen de deelnemers willekeurig om de dag 400 IE vitamine E gedurende een algemeen gemiddelde van 10.3 (13.8) jaar. Suppletie met vitamine E had geen onmiddellijke of langetermijneffecten op het risico op totale kanker of PCa [115]. Een matige dosis vitamine E-supplement (50 mg of ongeveer 75 IE) resulteerde echter in een lager PCa-risico bij 29,133 Finse mannelijke rokers [116]. Meerdere preklinische studies suggereren dat vitamine E de groei van tumoren vertraagt, deels door remming van de DNA-synthese en het induceren van apoptotische routes [117]. Helaas zijn studies bij mensen minder dan ondersteunend geweest. Twee observationele studies (de Cancer Prevention Study II Nutrition Cohort en de NIH-AARP Diet and Health Study) lieten beide geen verband zien tussen vitamine E-suppletie en PCa-risico [118,119]. Echter, een hoger serum β-tocoferol maar niet het β-tocoferol niveau was geassocieerd met een verminderd risico op PCa [120,121] en de associatie kan worden gewijzigd door genetische variaties in vitamine E-gerelateerde genen [122]. Integendeel, een prospectieve gerandomiseerde studie, de Selenium and Vitamin E Cancer Prevention Trial (SELECT), toonde aan dat vitamine E-suppletie het PCa-risico aanzienlijk verhoogde [123] en dat een hogere plasma-β-tocoferolspiegel kan interageren met seleniumsupplementen om het hoogwaardige PCa-risico te verhogen [124]. Deze bevinding komt overeen met een casus-cohortstudie van 1,739 gevallen en 3,117 controles die aantoonden dat vitamine E het PCa-risico verhoogde bij mensen met een lage seleniumstatus maar niet bij degenen met een hoge seleniumstatus [125]. Er is dus meer onderzoek nodig om de associatie tussen vitamine E en PCa te onderzoeken en het dosiseffect en de interactie met andere voedingsstoffen moeten worden overwogen.
Van vitamine K wordt verondersteld dat het PCa helpt voorkomen door het biologisch beschikbare calcium te verminderen. Preklinische studies tonen aan dat de combinatie van vitamine C en K in vitro krachtige antitumoractiviteit heeft en in vivo werkt als chemo- en radiosensibilisatoren [126]. Tot op heden hebben weinig studies dit onderzocht, hoewel een studie met behulp van het European Prospective Investigation into Cancer and Nutrition (EPIC)-Heidelberg-cohort een omgekeerd verband vond tussen de inname van vitamine K (als menaquinonen) en de incidentie van PCa [127]. Er zijn weinig tot geen preklinische studies uitgevoerd om de rol van calcium bij PCa te onderzoeken. Retrospectieve en meta-analyses suggereren een verhoogd of verlaagd PCa-risico met verhoogde calciuminname, terwijl andere geen verband suggereren [128,129]. Een andere studie suggereert een U-vormige associatie, waarbij zeer lage calciumspiegels of suppletie beide geassocieerd zijn met PCa [130].
Van selenium wordt daarentegen verondersteld dat het PCa voorkomt. Hoewel in-vitro-onderzoeken suggereerden dat selenium angiogenese en proliferatie remde terwijl het apoptose veroorzaakte [131], lieten de resultaten van SELECT geen voordeel zien van selenium alleen of in combinatie met vitamine E voor PCa-chemopreventie [123]. Verder kwam seleniumsuppletie niet ten goede aan mannen met een lage seleniumstatus, maar verhoogde het het risico op hoogwaardige PCa bij mannen met een hoge seleniumstatus in een willekeurig geselecteerd cohort van 1,739 gevallen met hoogwaardige (Gleason 7) PCa en 10 controles [ 3,117]. Een prospectieve Nederlandse cohortstudie, waaraan 125 mannen van 58,279 tot 55 jaar deelnamen, toonde ook aan dat teennagelselenium geassocieerd was met een verminderd risico op geavanceerde PCa [69]. Verder onderzoek is nodig om de rol van selenium bij PCa te verduidelijken.
fytochemicaliën
Samen met vitamines en mineralen [2] bevatten planten fytochemicaliën met potentiële kankerbestrijdende effecten. Doorgaans niet beschouwd als essentiële verbindingen, hebben fytochemicaliën antioxiderende en ontstekingsremmende eigenschappen.
Silibinin is een polyfenolische flavonoïde die voorkomt in de zaden van Mariadistel. In vitro en in vivo is aangetoond dat het de groei van PCa remt door zich te richten op epidermale groeifactorreceptor (EGFR), IGF-1-receptor (IGF-1R) en nucleaire factor-kappa B (NF-kB)-routes [133,134]. Een recente studie toonde aan dat silibinine nuttig kan zijn bij de preventie van PCa door remming van TGF?2-expressie en kankergeassocieerde fibroblast (CAF)-achtige biomarkers in stromale cellen van de menselijke prostaat [135]. Zodoende is silibinine een veelbelovende kandidaat als PCa-chemopreventief middel dat verder onderzoek wacht.
Curcumine wordt in Azië gebruikt als voedseladditief en als kruidengeneesmiddel tegen ontstekingen [136]. In vitro remt curcumine het pro-inflammatoire eiwit NF-βB terwijl het apoptose induceert door verhoogde expressie van proapoptotische genen [137]. In vivo vertraagt curcumine de groei van PCa bij muizen, terwijl het tumoren gevoelig maakt voor chemo- en radiotherapie [136]; geen enkele menselijke proef heeft echter de impact ervan op PCa onderzocht.
Granaatappel
De schil en het fruit van granaatappels en walnoten zijn rijk aan ellagitannines (punicalagins). Deze fytochemicaliën worden gemakkelijk gemetaboliseerd tot de actieve vorm ellaginezuur door de darmflora [138]. Preklinische experimenten tonen aan dat ellagitanninen PCa-proliferatie en angiogenese onder hypoxische omstandigheden remmen en apoptose induceren [137,138]. In prospectieve onderzoeken bij mannen met een stijgende PSA na primaire behandeling, verhoogde granaatappelsap of POMx, een in de handel verkrijgbaar granaatappelextract, de PSA-verdubbelingstijd ten opzichte van de uitgangswaarde [139,140], hoewel er geen onderzoeken waren met een placebogroep. De resultaten zijn in afwachting van een prospectieve placebo-RCT met gebruik van granaatappelextract bij mannen met een stijgende PSA. In een placebogecontroleerd onderzoek hadden twee pillen POMx per dag tot vier weken voorafgaand aan radicale prostatectomie echter geen invloed op tumorpathologie of oxidatieve stress of andere tumormaatregelen [141].
Groene thee
Groene thee bevat een aantal antioxidante polyfenolen, waaronder catechines, zoals epigallocatechinegallaat (EGCG), epigallocatechine (EGC), (?)-epicatechin-3-gallaat (ECG) en (?)-epicatechin. Preklinische studies suggereren dat EGCG PCa-groei remt, intrinsieke en extrinsieke apoptotische routes induceert en ontsteking vermindert door NFkB te remmen [137]. Bovendien zijn de antioxiderende eigenschappen van EGCG 25 tot 100 keer krachtiger dan vitamine C en E [131]. In een prospectieve gerandomiseerde preprostatectomie-studie consumeerden mannen die gebrouwen groene thee Lin et al. BMC Medicine (2015) 13:3 Pagina 7 van 15 hadden vóór de operatie verhoogde niveaus van polyfenolen uit groene thee in hun prostaatweefsel [142]. In een kleine proof-of-principle-studie met 60 mannen verminderde dagelijkse suppletie van 600 mg groene thee catechine-extract de incidentie van PCa met 90% (3% versus 30% in de placebogroep) [143]. Een ander klein onderzoek toonde ook aan dat EGCG-supplement resulteerde in een significante vermindering van PSA, hepatocytgroeifactor en vasculaire endotheliale groeifactor bij mannen met PCa [144]. Deze onderzoeken suggereren dat polyfenolen uit groene thee de incidentie van PCa kunnen verlagen en de progressie van PCa kunnen verminderen, maar er is meer onderzoek nodig om het mechanisme ervan te bevestigen en te verduidelijken [137,143,145].
Resveratrol
Hoewel de meeste in-vitro-onderzoeken suggereren dat resveratrol de groei van PCa remt [146-148], onderdrukt resveratrol de tumorgroei in sommige [137] maar niet alle diermodellen [149], mogelijk vanwege de beperkte biologische beschikbaarheid [150,151]. Tot op heden zijn er geen klinische onderzoeken die de preventieve of therapeutische effecten van resveratrol op PCa onderzoeken.
Zyflamend
Zyflamend is een ontstekingsremmend mengsel van kruiden waarvan is aangetoond dat het de progressie van PCa vermindert door de expressie van markers zoals pAKT, PSA, histondeacetylasen en androgeenreceptor in diermodellen en PCa-cellijnen te verlagen [152-154]. Ondanks het antikankerpotentieel [155] zijn er maar heel weinig onderzoeken bij mensen uitgevoerd [156,157]. In een open-label fase I-onderzoek met 23 patiënten met hooggradige prostaat-intra-epitheliale neoplasie verminderde Zyflamend alleen of in combinatie met andere voedingssupplementen gedurende 18 maanden het risico op het ontwikkelen van PCa [156]. Er zijn meer RCT's bij mensen nodig om de werkzaamheid en klinische toepassing van dit kruidensupplement te bevestigen.
Andere Whole Foods Groenten en fruit
Groenten en fruit zijn rijke bronnen van vitamines, mineralen en fytochemicaliën. Verschillende epidemiologische onderzoeken vonden omgekeerde relaties tussen de totale inname van fruit en groenten [158] en de inname van kruisbloemige groenten en PCa-risico [159,160]. Alliumgroenten, zoals knoflook, prei, bieslook en sjalotten, bevatten meerdere zwavelhoudende fytochemicaliën waarvan werd gesuggereerd dat ze het immuunsysteem versterken, celgroei remmen, expressie van op androgeen reagerende genen moduleren en apoptose induceren [161]. Hoewel het aantal gepubliceerde onderzoeken beperkt is, suggereren zowel preklinische als epidemiologische gegevens dat de inname van alliumgroenten beschermend kan zijn tegen PCa, met name lokale ziekte [162]. Een gerandomiseerde studie met 199 mannen wees ook uit dat een gemengd supplement van granaatappel, groene thee, broccoli en kurkuma de stijging van PSA bij mannen met PCa aanzienlijk verminderde [163].
Tomaten & Tomatenproducten
Een aantal studies hebben de associatie tussen tomaten en tomatenproducten met PCa onderzocht, maar de bevindingen zijn niet doorslaggevend. Het antioxidant lycopeen, dat rijk is aan tomaten, is ook specifiek bestudeerd vanwege zijn impact op PCa. In vitro stopt lycopeen de celcyclus in verschillende PCa-cellijnen en vermindert IGF-1-signalering door IGF-1-bindende eiwitten te induceren [131]. Hoewel sommige dierstudies hebben aangetoond dat lycopeen specifiek de PCa-groei vertraagt [164] of PCa-epitheelcellen vermindert in stadia van initiatie, promotie en progressie [165], vonden twee onderzoeken tegenstrijdige bevindingen tussen tomatenpuree en lycopeen [166,167]. Prospectieve studies bij mensen vonden een hogere lycopeenconsumptie [168,169] of hogere serumspiegels waren geassocieerd met een lager PCa-risico [170], maar andere niet [171,172]. Prostaatlycopeenconcentratie onder een drempel van 1 ng/mg was geassocieerd met PCa na zes maanden follow-upbiopsie (P = 0.003) [173]. Twee kortlopende preprostatectomie-onderzoeken met tomatensaus of suppletie met lycopeen toonden de opname van lycopeen in prostaatweefsel en antioxiderende en mogelijke kankerbestrijdende effecten aan [174,175]. Hoewel verschillende klinische onderzoeken een omgekeerd verband suggereerden tussen suppletie met lycopeen, PSA-waarden en afname van kankergerelateerde symptomen [171,176], hebben geen grootschalige gerandomiseerde onderzoeken de rol van lycopeen- of tomatenproducten op PCa-preventie of -behandeling getest.
Koffie
Koffie bevat cafeïne en verschillende niet-geïdentificeerde fenolverbindingen die als antioxidanten kunnen dienen. Epidemiologische studies suggereren een omgekeerde relatie tussen koffieconsumptie en PCa-risico, voornamelijk voor ziekte in een gevorderd of dodelijk stadium, en de bevindingen waren onafhankelijk van het cafeïnegehalte [177,178]. Hoewel verschillende epidemiologische studies [179-182] geen verband vonden tussen koffieconsumptie en PCa-risico, concludeerde een recente meta-analyse van prospectieve studies dat koffieconsumptie het PCa-risico kan verminderen [183]. Het (de) mogelijke mechanisme(n) en route(s) die hierbij betrokken zijn, zijn onbekend, maar kunnen antioxiderende, ontstekingsremmende effecten, glucose- en insulinemetabolisme en mogelijke invloed op IGF-I en circulerende geslachtshormonen omvatten.
Dieetpatronen
Hoewel veel afzonderlijke voedingsstoffen of voedingsfactoren zijn onderzocht op hun impact of associatie met PCa-risico of -progressie, waren de resultaten grotendeels niet doorslaggevend. Een mogelijke reden voor de inconsistentie is het feit dat de impact van een enkele voedingsstof of voedingsfactor mogelijk te klein is om te worden gedetecteerd. Bovendien zijn voedingsstoffen die van nature in voedingsmiddelen voorkomen vaak sterk gecorreleerd en kunnen ze op elkaar inwerken en dus de impact op PCa beïnvloeden. Zo heeft de analyse van voedingspatronen een toenemende Lin et al. BMC Medicine (2015) 13:3 Pagina 8 van 15 maar het onderzoek is beperkt en de bestaande resultaten zijn niet doorslaggevend. In een cohort van 293,464 mannen was een hoge voedingskwaliteit, zoals aangegeven door de Healthy Eating Index (HEI)-score, geassocieerd met een lager risico op het totale PCa-risico [70]. Het mediterrane dieet, dat rijk is aan groenten, olijfolie, complexe koolhydraten, mager vlees en antioxidanten, wordt consequent aanbevolen aan patiënten ter voorkoming van cardiovasculaire aandoeningen en obesitas [184], en kan veelbelovend zijn bij PCa-preventie [185]. Vis- en omega-3-vetzuurconsumptie in het mediterrane patroon was significant en omgekeerd geassocieerd met fataal PCa-risico. Bovendien was het volgen van het mediterrane dieet na de diagnose van niet-gemetastaseerde PCa geassocieerd met een lagere algehele mortaliteit [186]. Terwijl een westers patroon met een hoge inname van rood vlees, vleeswaren, gebakken vis, chips, magere melk en witbrood geassocieerd was met een hoger risico op PCa [187].
Bovendien hebben Aziatische landen met een hoge consumptie van omega-3 PUFA's, soja en fytochemicaliën op basis van groene thee een lagere PCa-incidentie vergeleken met landen die een 'westers' dieet volgen [188]. Niet alle onderzoeken [189-191] ondersteunden echter een verband tussen een bepaald voedingspatroon en het risico op PCa. Het is mogelijk dat de methodologie die wordt gebruikt bij het identificeren van voedingspatronen niet alle voedingsfactoren bevat die verband houden met het PCa-risico. Als alternatief kan elk voedingspatroon zowel gunstige als schadelijke componenten bevatten, wat resulteert in een algehele nulassociatie. Er is meer onderzoek nodig om te blijven zoeken naar voedingspatronen die de meeste gunstige voedingsstoffen/voedingsfactoren voor PCa combineren en de meeste negatieve voedingsstoffen/voedingsfactoren beperken.
Toekomstige richting voor klinische proeven
Op basis van de veelheid aan epidemiologische, preklinische en klinische onderzoeken die in dit overzicht worden beschreven, zijn voedingsinterventies voor de preventie en behandeling van PCa veelbelovend. Bovendien kunnen verschillende voedingsfactoren en vitamines/supplementen in verband worden gebracht met het risico op PCa en/of de progressie van de ziekte. Prospectieve gerandomiseerde onderzoeken zijn duidelijk geïndiceerd om specifieke voedingsstoffen of combinatietherapieën te identificeren voor de preventie en behandeling van PCa.
Onlangs is actieve bewaking (AS) naar voren gekomen als een haalbare optie voor mannen met PCa met een lager risico. Mannen met AS zijn gemotiveerd om zich te houden aan veranderingen in het dieet en de levensstijl [192], waardoor deze subgroep een goed doelwit is voor voedingsinterventie en onderzoeken naar de kwaliteit van leven [193]. PCa-overlevenden die actiever zijn en 'gezonde' eetgewoonten rapporteren (dat wil zeggen, vetarme, laaggeraffineerde koolhydraatrijke diëten consumeren die rijk zijn aan fruit en groenten) hebben een betere algehele kwaliteit van leven dan hun inactieve, ongezonde tegenhangers [194]. Er zijn dus meer gerandomiseerde onderzoeken nodig om de algehele langetermijneffecten van voedingsinterventie bij deze populatie te bepalen. Concreet zijn de belangrijkste vragen die in toekomstige onderzoeken moeten worden beantwoord: 1) Kunnen voedingsinterventies de noodzaak van behandeling bij mannen met AS vertragen; 2) Kunnen voedingsinterventies herhaling bij mannen na behandeling voorkomen; 3) Kunnen voedingsinterventies de progressie bij mannen met terugkerende ziekte vertragen en zo de behoefte aan hormonale therapie vertragen; 4) Kunnen voedingsinterventies de bijwerkingen van PCa-behandelingen verminderen, waaronder hormoontherapie en nieuwere gerichte therapieën; en 5) Is er een rol weggelegd voor voedingsinterventies alleen of in combinatie met gerichte therapieën bij mannen die hormonale therapie krijgen om castratieresistentie te voorkomen of na het ontstaan van castratieresistentie? Omdat toenemend bewijs aantoont dat metabole afwijkingen het risico op PCa verhogen, is leefstijlinterventie die het metabole profiel verbetert een win-winoptie voor PCa-preventie en -behandeling [195,196].
Conclusies: prostaatkanker
Toekomstig onderzoek is nodig om het ideale dieet voor PCa-preventie of -behandeling te bepalen. Verschillende voedingsfactoren en sommige voedingspatronen zijn echter veelbelovend in het verminderen van PCa-risico of -progressie en zijn consistent met de huidige voedingsrichtlijnen voor Amerikanen [197]. Voor het adviseren van patiënten over een dieet voor primaire en secundaire PCa-preventie, geloven velen dat "gezond hart gelijk staat aan gezonde prostaat". koolhydraten met volle granen, het verminderen van totaal en verzadigd vet, het verminderen van te gaar vlees en het consumeren van een matige hoeveelheid calorieën of het verminderen van koolhydraten met als hoofddoel het verkrijgen en behouden van een gezond lichaamsgewicht.
Concurrerende belangen De auteurs verklaren dat zij geen concurrerende belangen hebben.
Auteursbijdragen P-HL en SF voerden de review uit, P-HL stelde het manuscript op en SF en WA redigeerden en leverden kritische input. Alle auteurs hebben het definitieve manuscript gelezen en goedgekeurd.
Dankbetuigingen De financiering werd verstrekt door subsidies 1K24CA160653 (Freedland), NIH P50CA92131 (W. Aronson). Dit manuscript is het resultaat van werk ondersteund met middelen en het gebruik van faciliteiten in het Veterans Administration Medical Center, West Los Angeles (W. Aronson).
Auteursgegevens 1 Department of Medicine, Division of Nephrology, Duke University Medical Center, Box 3487, Durham, NC 27710, VS. 2 Afdeling Urologie, Afdeling Chirurgie, Veteranenzaken Greater Los Angeles Healthcare System, Los Angeles, CA, VS. 3 Afdeling Urologie, UCLA School of Medicine, Los Angeles, CA, VS. 4 Sectie Urologie, Afdeling Chirurgie, Durham Veterans Affairs Medical Center, Afdeling Urologie, Durham, NC, VS. 5 Duke Prostate Center, Afdelingen Chirurgie en Pathologie, Duke University Medical Center, Durham, NC, VS.
blanco
Referenties:
1. Centrum MM, Jemal A, Lortet-Tieulent J, Ward E, Ferlay J, Brawley O, Bray F:
Internationale variatie in incidentie van prostaatkanker en sterftecijfers.
Eur Urol 2012, 61:1079�1092.
2. Masko EM, Allott EH, Freedland SJ: de relatie tussen voeding en
prostaatkanker: is meer altijd beter? Eur Urol 2013, 63:810�820.
3. Mavropoulos JC, Isaacs WB, Pizzo SV, Freedland SJ: Is er een rol weggelegd voor een
koolhydraatarm ketogeen dieet bij de behandeling van prostaatkanker?
Urologie 2006, 68:15�18.
4. Freedland SJ, Mavropoulos J, Wang A, Darshan M, Demark-Wahnefried W,
Aronson WJ, Cohen P, Hwang D, Peterson B, Velden T, Pizzo SV, Isaacs WB:
Beperking van koolhydraten, groei van prostaatkanker en het insuline-achtige
groeifactor as. Prostaat 2008, 68:11�19.
5. Mavropoulos JC: Buschemeyer WC 3e, Tewari AK, Rokhfeld D, Pollak M,
Zhao Y, Febbo PG, Cohen P, Hwang D, Devi G, Demark-Wahnefried W,
Westman EC, Peterson BL, Pizzo SV, Freedland SJ: de effecten van variëren
koolhydraat- en vetgehalte in de voeding op overleving in een muizen-LNCaP
xenotransplantaatmodel voor prostaatkanker. Kanker Prev Res (Phila Pa) 2009,
2: 557.
6. Masko EM, Thomas JA 2e, Antonelli JA, Lloyd JC, Phillips TE, Poulton SH,
Dewhirst MW, Pizzo SV, Freedland SJ: Koolhydraatarme diëten en
prostaatkanker: hoe laag is 'laag genoeg'? Kanker Prev Res (Phila) 2010,
3: 1124.
7. Drake I, Sonestedt E, Gullberg B, Ahlgren G, Bjartell A, Wallstrom P, Wirfült E:
Voedingsinname van koolhydraten in relatie tot het risico op prostaatkanker:
prospectieve studie in het Malmo Diet and Cancer-cohort. Ben J Clin Nutr
2012, 96:1409-1418.
8. Zhang J, Shen C, Wang L, Ma Q, Xia P, Qi M, Yang M, Han B: Metformine
remt epitheel-mesenchymale overgang in prostaatkankercellen:
Betrokkenheid van de tumoronderdrukker miR30a en zijn doelgen SOX4.
Biochem Biophys Res Commun 2014, 452:746-752.
9. Lee SY, Song CH, Xie YB, Jung C, Choi HS, Lee K: SMILE opgereguleerd door
metformine remt de functie van de androgeenreceptor bij prostaatkanker
cellen. Kreeft Lett 2014, 354:390�397.
10. Demir U, Koehler A, Schneider R, Schweiger S, Klocker H: metformine antitumor
effect via verstoring van het MID1 translationele regulatorcomplex
en AR-downregulatie in prostaatkankercellen. BMC Kanker 2014, 14:52.
11. Margel D: Metformine om prostaatkanker te voorkomen: een oproep om ons te verenigen. Euro Urol
2014. doi:10.1016/j.eururo.2014.05.012. [Epub van tevoren]
12. Margel D, Urbach DR, Lipscombe LL, Bell CM, Kulkarni G, Austin PC, Fleshner
N: gebruik van metformine en mortaliteit door alle oorzaken en prostaatkanker
bij mannen met diabetes. J Clin Oncol 2013, 31:3069�3075.
13. Tseng CH: Metformine vermindert het risico op prostaatkanker aanzienlijk
bij Taiwanese mannen met diabetes mellitus type 2. Eur J Kreeft 2014,
50: 2831.
14. Joshua AM, Zannella VE, Downes MR, Bowes B, Hersey K, Koritzinsky M,
Schwab M, Hofmann U, Evans A, van der Kwast T, Trachtenberg J, Finelli A,
Fleshner N, Sweet J, Pollak M: een pilot 'window of opportunity'
neoadjuvante studie van metformine bij gelokaliseerde prostaatkanker. Prostaat
Kanker Prostaat Dis 2014, 17:252�258.
15. Rothermundt C, Hayoz S, Templeton AJ, Winterhalder R, Strebel RT, Bartschi
D, Pollak M, Lui L, Endt K, Schiess R, R�schoff JH, Cathomas R, Gillessen S:
Metformine bij chemotherapie-naïeve castratieresistente prostaatkanker:
Een multicenter fase 2-onderzoek (SAKK 08/09). Eur Urol 2014, 66:468�474.
16. Allott EH, Abern MR, Gerber L, Keto CJ, Aronson WJ, Terris MK, Kane CJ,
Amling CL, Cooperberg MR, Moorman PG, Freedland SJ: Metformine wel
geen invloed op het risico van biochemisch recidief na radicaal
prostatectomie: resultaten uit de SEARCH-database. Prostaatkanker
Prostaat Dis 2013, 16:391�397.
17. Rieken M, Kluth LA, Xylinas E, Fajkovic H, Becker A, Karakiewicz PI, Herman
M, Lotan Y, Seitz C, Schramek P, Remzi M, Loidl W, Pummer K, Lee RK,
Faison T, Scherr DS, Kautzky-Willer A, Bachmann A, Tewari A, Shariat SF:
Associatie van diabetes mellitus en metforminegebruik met biochemisch
recidief bij patiënten die een radicale prostatectomie voor de prostaat hebben ondergaan
kanker. Wereld J Urol 2014, 32:999�1005.
18. Margel D, Urbach D, Lipscombe LL, Bell CM, Kulkarni G, Austin PC, Fleshner
N: Associatie tussen metforminegebruik en risico op prostaatkanker en
zijn cijfer. J Natl Kanker Inst 2013, 105:1123�1131.
19. Franciosi M, Lucisano G, Lapice E, Strippoli GF, Pellegrini F, Nicolucci A:
Metforminetherapie en risico op kanker bij patiënten met diabetes type 2:
systematische herziening. PLoS One 2013, 8:e71583.
20. Kaushik D, Karnes RJ, Eisenberg MS, Rangel LJ, Carlson RE, Bergstralh EJ:
Effect van metformine op de uitkomsten van prostaatkanker na radicaal
prostatectomie. Urol Oncol 2014, 32:43 e41�47.
21. Bensimon L, Yin H, Suissa S, Pollak MN, Azoulay L: het gebruik van metformine in
patiënten met prostaatkanker en het risico op overlijden. Kanker Epidemiol
Biomarkers Vorige 2014, 23:2111�2118.
22. Tsilidis KK, Capothanassi D, Allen NE, Rizos EC, Lopez DS, van Veldhoven K,
Sacerdote C, Ashby D, Vineis P, Tzoulaki I, Ioannidis JP: Metformine werkt niet
het risico op kanker beïnvloeden: een cohortstudie in het UK Clinical Practice Research
Datalink geanalyseerd als een intention-to-treat-onderzoek. Diabeteszorg 2014,
37: 2522.
23. Levine ME, Suarez JA, Brandhorst S, Balasubramanian P, Cheng CW, Madia F,
Fontana L, Mirisola MG, Guevara-Aguirre J, Wan J, Passarino G, Kennedy BK,
Wei M, Cohen P, Crimmins EM, Longo VD: er is een verband met een lage eiwitinname
met een grote vermindering van IGF-1, kanker en algehele mortaliteit in de 65
en jongere maar niet oudere bevolking. Cel Metab 2014, 19:407�417.
24. Solon-Biet SM, McMahon AC, Ballard JW, Ruohonen K, Wu LE, Cogger VC,
Warren A, Huang X, Pichaud N, Melvin RG, Gokarn R, Khalil M, Turner N,
Cooney GJ, Sinclair DA, Raubenheimer D, Le Couteur DG, Simpson SJ: De
verhouding van macronutriënten, niet calorie-inname, dicteert cardiometabool
gezondheid, veroudering en levensduur bij ad libitum gevoede muizen. Cel Metab 2014,
19: 418.
25. Richman EL, Stampfer MJ, Paciorek A, Broering JM, Carroll PR, Chan JM:
Inname van vlees, vis, gevogelte en eieren en risico op prostaatkanker
progressie. Am J Clin Nutr 2010, 91:712�721.
26. Joshi AD, John EM, Koo J, Ingles SA, Stern MC: Visopname, koken
praktijken en risico op prostaatkanker: resultaten van een multi-etnische
case-control studie. Kanker veroorzaakt controle 2012, 23:405�420.
27. Joshi AD, Corral R, Catsburg C, Lewinger JP, Koo J, John EM, Ingles SA,
Stern MC: Rood vlees en gevogelte, kookpraktijken, genetische vatbaarheid
en risico op prostaatkanker: resultaten van een multi-etnische casuscontrole
studie. Kankerverwekkendheid 2012, 33:2108-2118.
28. Catsburg C, Joshi AD, Corral R, Lewinger JP, Koo J, John EM, Ingles SA,
Stern MC: polymorfismen in carcinogene metabolisme-enzymen, vissen
inname en risico op prostaatkanker. Kankerverwekkendheid 2012, 33:1352-1359.
29. Pettersson A, Kasperzyk JL, Kenfield SA, Richman EL, Chan JM, Willett WC,
Stampfer MJ, Mucci LA, Giovannucci EL: melk- en zuivelconsumptie
bij mannen met prostaatkanker en risico op uitzaaiingen en prostaatkanker
kanker dood. Kanker Epidemiol Biomarkers Vorige 2012, 21:428�436.
30. Deneo-Pellegrini H, Ronco AL, De Stefani E, Boffetta P, Correa P,
Mendilaharsu M, Acosta G: Voedselgroepen en risico op prostaatkanker: een
case-control studie in Uruguay. Kanker veroorzaakt controle 2012, 23:1031�1038.
31. Park SY, Murphy SP, Wilkens LR, Stram DO, Henderson BE, Kolonel LN:
Inname van calcium, vitamine D en zuivelproducten en risico op prostaatkanker:
de multi-etnische cohortstudie. Am J Epidemiol 2007, 166:1259-1269.
32. Lied Y, Chavarro JE, Cao Y, Qiu W, Mucci L, Sesso HD, Stampfer MJ,
Giovannucci E, Pollak M, Liu S, Ma J: Inname van volle melk wordt geassocieerd met
prostaatkankerspecifieke mortaliteit onder Amerikaanse mannelijke artsen. J Nutr febr
2013, 143:189-196.
33. Jonge NJ, Metcalfe C, Gunnell D, Rowlands MA, Lane JA, Gilbert R, Avery
KN, Davis M, Neal DE, Hamdy FC, Donovan J, Martin RM, Holly JM: een dwarsdoorsnede
analyse van het verband tussen voeding en insulineachtige groei
factor (IGF)-I, IGF-II, IGF-bindend eiwit (IGFBP)-2 en IGFBP-3 bij mannen in
het Verenigd Koninkrijk. Kanker veroorzaakt controle 2012, 23:907-917.
34. Christensen MJ, Quiner TE, Nakken HL, Lephart ED, Eggett DL, Urie PM:
Combinatie-effecten van soja in de voeding en methylselenocysteïne bij een muis
model van prostaatkanker. Prostaat 2013, 73:986�995.
35. Bosland MC, Kato I, Zeleniuch-Jacquotte A, Schmoll J, Enk Rueter E,
Melamed J, Kong MX, Macias V, Kajdacsy-Balla A, Lumey LH, Xie H, Gao W,
Walden P, Lepor H, Taneja SS, Randolph C, Schlicht MJ, Meserve-Watanabe
H, Deaton RJ, Davies JA: Effect van suppletie met soja-eiwitisolaat op
biochemisch recidief van prostaatkanker na radicale prostatectomie: a
gerandomiseerde proef. JAMA 2013, 310:170�178.
36. Chiyomaru T, Yamamura S, Fukuhara S, Yoshino H, Kinoshita T, Majid S, Saini
S, Chang I, Tanaka Y, Enokida H, Seki N, Nakagawa M, Dahiya R: Genisteïne
remt de groei van prostaatkankercellen door zich te richten op miR-34a en oncogeen
HETE LUCHT. PLoS One 2013, 8:e70372.
37. Zhang S, Wang Y, Chen Z, Kim S, Iqbal S, Chi A, Ritenour C, Wang YA, Kucuk
O, Wu D: Genisteïne verbetert de werkzaamheid van cabazitaxel-chemotherapie
in uitgezaaide castratieresistente prostaatkankercellen. Prostaat 2013,
73:1681�1689.38. van Die MD, Bone KM, Williams SG, Pirotta MV: Soja en soja-isoflavonen in
prostaatkanker: een systematische review en meta-analyse van gerandomiseerde
gecontroleerde proeven. BJU Int 2014, 113:E119�E130.
39. Hamilton-Reeves JM, Banerjee S, Banerjee SK, Holzbeierlein JM, Thrasher JB,
Kambhampati S, Keighley J, Van Veldhuizen P: Soja-isoflavon op korte termijn
interventie bij patiënten met gelokaliseerde prostaatkanker: een gerandomiseerde,
dubbelblinde, placebogecontroleerde studie. PLoS One 2013, 8:e68331.
40. Pavese JM, Krishna SN, Bergan RC: Genisteïne remt de menselijke prostaat
onthechting, invasie en metastase van kankercellen. Ben J Clin Nutr 2014,
100:431S-436S.
41. Gonzalez-Menendez P, Hevia D, Rodriguez-Garcia A, Mayo JC, Sainz RM:
Regulatie van GLUT-transporters door flavonoïden in androgeengevoelige en
-ongevoelige prostaatkankercellen. Endocrinologie 2014, 155:3238�3250.
42. Hirata H, Hinoda Y, Shahryari V, Deng G, Tanaka Y, Tabatabai ZL, Dahiya R:
Genisteïne reguleert onco-miR-1260b en reguleert sFRP1 en
Smad4 via demethylering en histon-modificatie bij prostaatkanker
cellen. Br J Kreeft 2014, 110:1645�1654.
43. Handayani R, Rijst L, Cui Y, Medrano TA, Samedi VG, Baker HV, Szabo NJ,
Shiverick KT: Soja-isoflavonen veranderen de expressie van genen die geassocieerd zijn met
kankerprogressie, inclusief interleukine-8, in androgeenonafhankelijk
PC-3 menselijke prostaatkankercellen. J Nutr 2006, 136:75�82.
44. Travis RC, Allen NE, Appleby PN, Prijs A, Kaaks R, Chang-Claude J, Boeing H,
Aleksandrova K, Tj�nneland A, Johnsen NF, Overvad K, Ram�n Quir�s J,
Gonz�lez CA, Molina-Montes E, S�nchez MJ, Larra�aga N, Casta�o JM,
Ardanaz E, Khaw KT, Wareham N, Trichopoulou A, Karapetyan T, Rafnsson
SB, Palli D, Krogh V, Tumino R, Vineis P, Bueno-de-Mesquita HB, Stattin P,
Johansson M, et al: Prediagnostische concentraties van genisteïne in plasma en
risico op prostaatkanker bij 1,605 mannen met prostaatkanker en 1,697
gematchte controledeelnemers in EPIC. Kanker veroorzaakt controle 2012,
23: 1163.
45. Jackson MD, McFarlane-Anderson ND, Simon GA, Bennett FI, Walker SP:
Urine-fyto-oestrogenen en risico op prostaatkanker bij Jamaicaanse mannen.
Kanker veroorzaakt controle 2010, 21:2249�2257.
46. Lazarevic B, Hammarström C, Yang J, Ramberg H, Diep LM, Karlsen SJ,
Kucuk O, Saatcioglu F, Task�n KA, Svindland A: De effecten van
genisteïne-interventie op prostaatbiomarker-expressie bij patiënten met
gelokaliseerde prostaatkanker vóór radicale prostatectomie. Br J Nutr 2012,
108: 2138.
47. Epstein MM, Kasperzyk JL, Mucci LA, Giovannucci E, Prijs A, Wolk A,
H�kansson N, Fall K, Andersson SO, Andr�n O: vetzuurinname via de voeding en
overleving van prostaatkanker in Orebro County, Zweden. Am J Epidemiol 2012,
176: 240.
48. Kobayashi N, Barnard RJ, Said J, Hong-Gonzalez J, Corman DM, Ku M,
Doan NB, Gui D, Elashoff D, Cohen P, Aronson WJ: Effect van vetarm dieet op
ontwikkeling van prostaatkanker en Akt-fosforylering in de Hi-Myc
transgeen muismodel. Kankeronderzoek 2008, 68:3066�3073.
49. Ngo TH, Barnard RJ, Cohen P, Freedland S, Tran C, deGregorio F, Elshimali
YI, Heber D, Aronson WJ: Effect van isocalorisch vetarm dieet op de mens
LAPC-4 prostaatkanker xenotransplantaten bij ernstige gecombineerde immunodeficiëntie
muizen en de insuline-achtige groeifactor-as. Clin Kankeronderzoek 2003,
9: 2734.
50. Huang M, Narita S, Numakura K, Tsuruta H, Saito M, Inoue T, Horikawa Y,
Tsuchiya N, Habuchi T: Een vetrijk dieet bevordert de proliferatie van
prostaatkankercellen en activeert MCP-1/CCR2-signalering. Prostaat 2012,
72: 1779.
51. Chang SN, Han J, Abdelkader TS, Kim TH, Lee JM, Song J, Kim KS, Park JH,
Park JH: Hoge inname van dierlijk vet bevordert de progressie van prostaatkanker
en vermindert de expressie van glutathionperoxidase 3 in de vroege stadia van
TRAMP muizen. Prostaat 2014, 74:1266�1277.
52. Bidoli E, Talamini R, Bosetti C, Negri E, Maruzzi D, Montella M, Franceschi S,
La Vecchia C: Macronutriënten, vetzuren, cholesterol en prostaatkanker
risico. Ann Oncol 2005, 16:152�157.
53. Park SY, Murphy SP, Wilkens LR, Henderson BE, Kolonel LN: vet en vlees
inname en risico op prostaatkanker: de multi-etnische cohortstudie. Int J Kanker
2007, 121:1339-1345.
54. Wallstrom P, Bjartell A, Gullberg B, Olsson H, Wirfalt E: een prospectieve studie
over vet in de voeding en de incidentie van prostaatkanker (Malmö, Zweden).
Kanker veroorzaakt controle 2007, 18:1107�1121.
55. Crowe FL, Key TJ, Appleby PN, Travis RC, Overvad K, Jakobsen MU,
Johnsen NF, Tj�nneland A, Linseisen J, Rohrmann S, Boeing H, Pischon T,
Trichopoulou A, Lagiou P, Trichopoulos D, Sacerdote C, Palli D, Tumino R,
Krogh V, Bueno-de-Mesquita HB, Kiemeney LA, Chirlaque MD, Ardanaz E,
S�nchez MJ, Larra�aga N, Gonz�lez CA, Quir�s JR, Manjer J, Wirf�lt E, Stattin
P, et al: Vetinname via de voeding en risico op prostaatkanker in de Europeaan
Prospectief onderzoek naar kanker en voeding. Ben J Clin Nutr 2008,
87: 1405.
56. Ohwaki K, Endo F, Kachi Y, Hattori K, Muraishi O, Nishikitani M, Yano E:
Relatie tussen voedingsfactoren en prostaatspecifiek antigeen in
gezonde mannen. Urol Int 2012, 89:270�274.
57. Bassett JK, Severi G, Hodge AM, MacInnis RJ, Gibson RA, Hopper JL,
Engels DR, Giles GG: Plasmafosfolipidenvetzuren, voedingsvetzuren
en het risico op prostaatkanker. Int J Kanker 2013, 133:1882-1891.
58. Richman EL, Kenfield SA, Chavarro JE, Stampfer MJ, Giovannucci EL, Willett
WC, Chan JM: Vetinname na diagnose en risico op dodelijke prostaatkanker
en sterfte door alle oorzaken. JAMA Intern Med 2013, 173:1318�1326.
59. Williams CD, Whitley BM, Hoyo C, Grant DJ, Iraggi JD, Newman KA, Gerber
L, Taylor LA, McKeever MG, Freedland SJ: een hoge verhouding van n-6 / n-3 via de voeding
meervoudig onverzadigde vetzuren wordt in verband gebracht met een verhoogd risico op prostaat
kanker. Nutr Res 2011, 31:1�8.
60. Chua ME, Sio MC, Sorongon MC, Dy JS: relatie tussen inname via de voeding van
omega-3- en omega-6-vetzuren met risico op prostaatkanker
ontwikkeling: een meta-analyse van prospectieve studies en beoordeling van
literatuur. Prostaatkanker 2012, 2012:826254.
61. Berquin IM, Edwards IJ, Kridel SJ, Chen YQ: meervoudig onverzadigd vetzuur
stofwisseling bij prostaatkanker. Kankermetastase Rev 2011, 30:295�309.
62. Aronson WJ, Kobayashi N, Barnard RJ, Henning S, Huang M, Jardack PM, Liu
B, Grey A, Wan J, Konijeti R, Freedland SJ, Castor B, Heber D, Elashoff D, Said
J, Cohen P, Galet C: Fase II prospectieve gerandomiseerde studie van een vetarm dieet
met visoliesuppletie bij mannen die radicale prostatectomie ondergaan.
Kanker Prev Res (Phila) 2011, 4:2062-2071.
63. Hughes-Fulford M, Li CF, Boonyaratanakornkit J, Sayyah S: Arachidonzuur
activeert fosfatidylinositol 3-kinase signalering en induceert gen
expressie bij prostaatkanker. Kankeronderzoek 2006, 66:1427-1433.
64. Moreel X, Allaire J, Leger C, Caron A, Labonte ME, Lamarche B, Julien P,
Desmeules P, T�tu B, Fradet V: Prostaat- en omega-3-vetzuren in de voeding
en progressie van prostaatkanker tijdens actief toezicht. Kanker Vorige
Onderzoek (Phila) 2014, 7: 766-776.
65. Spencer L, Mann C, Metcalfe M, Webb M, Pollard C, Spencer D, Berry D,
Steward W, Dennison A: Het effect van omega-3 FA's op tumorangiogenese
en hun therapeutisch potentieel. Eur J Kanker 2009, 45:2077�2086.
66. Gu Z, Suburu J, Chen H, Chen YQ: mechanismen van omega-3 meervoudig onverzadigd
vetzuren bij de preventie van prostaatkanker. Biomed Res Int 2013, 2013:824563.
67. Lloyd JC, Masko EM, Wu C, Keenan MM, Pilla DM, Aronson WJ, Chi JT,
Freedland SJ: Visolie vertraagt de groei van prostaatkanker xenograft ten opzichte van
andere voedingsvetten en wordt geassocieerd met verminderde mitochondriale en
genexpressie van de insulineroute. Prostaatkanker Prostaat Dis 2013,
16: 285.
68. Williams CM, Burdge G: n-3 PUFA met lange keten: plant v. mariene bronnen.
Proc Nutr Soc 2006, 65:42.
69. Galet C, Gollapudi K, Stepanian S, Byrd JB, Henning SM, Grogan T, Elashoff
D, Heber D, Said J, Cohen P, Aronson WJ: Effect van een vetarm visoliedieet
op pro-inflammatoire eicosanoïden en celcyclusprogressiescore in
mannen die een radicale prostatectomie ondergaan. Kanker Prev Res (Phila) 2014,
7: 97.
70. Bosire C, Stampfer MJ, Subar AF, Park Y, Kirkpatrick SI, Chiuve SE, Hollenbeck
AR, Reedy J: op indexen gebaseerde voedingspatronen en het risico op prostaatkanker
in de NIH-AARP studie naar voeding en gezondheid. Am J Epidemiol 2013, 177:504-513.
71. Aronson WJ, Barnard RJ, Freedland SJ, Henning S, Elashoff D, Jardack PM,
Cohen P, Heber D, Kobayashi N: groeiremmend effect van een vetarm dieet
op prostaatkankercellen: resultaten van een prospectief, gerandomiseerd dieet
interventiestudie bij mannen met prostaatkanker. J Urol 2010, 183:345�350.
72. Brouwer IA, Geleijnse JM, Klaasen VM, Smit LA, Giltay EJ, de Goede J,
Heijboer AC, Kromhout D, Katan MB: Effect van alfa-linoleenzuur
suppletie op serum prostaatspecifiek antigeen (PSA): resultaten van
de alfa-omega-proef. PLoS One 2013, 8:e81519.
73. Chua ME, Sio MC, Sorongon MC, Morales ML Jr: de relevantie van serum
niveaus van langketenige omega-3 meervoudig onverzadigde vetzuren en prostaat
risico op kanker: een meta-analyse. Kan Urol Assoc J 2013, 7:E333�E343.
74. Yue S, Li J, Lee SY, Lee HJ, Shao T, Lied B, Cheng L, Masterson TA, Liu X,
Ratliff TL, Cheng JX: Cholesterylesteraccumulatie veroorzaakt door PTEN-verlies
en PI3K/AKT-activering ligt ten grondslag aan prostaatkanker bij de mens
agressiviteit. Cel Metab 2014, 19:393�406.
75. Sun Y, Sukumaran P, Varma A, Derry S, Sahmoun AE, Singh BB: Cholesterolgeïnduceerd
activering van TRPM7 reguleert celproliferatie, migratie,
en levensvatbaarheid van menselijke prostaatcellen. Biochim Biophys Acta 1843,
2014: 1839.
76. Murai T: Cholesterolverlaging: rol bij de preventie en behandeling van kanker.
Biol Chem 2014. doi:10.1515/hsz-2014-0194. [Epub van tevoren]
77. Zhuang L, Kim J, Adam RM, Solomon KR, Freeman MR: cholesterol
targeting verandert de samenstelling van het lipide-vlot en de celoverleving bij prostaatkanker
cellen en xenotransplantaten. J Clin Invest 2005, 115:959-968.
78. Mostaghel EA, Solomon KR, Pelton K, Freeman MR, Montgomery RB:
Impact van circulerend cholesterolgehalte op groei en intratumoraal
androgeenconcentratie van prostaattumoren. PLoS One 2012,
7: e30062.
79. Morote J, Celma A, Planas J, Placer J, de Torres I, Olivan M, Carles J,
Revent's J, Doll A: rol van serumcholesterol en statinegebruik bij het risico van
prostaatkankerdetectie en tumoragressiviteit. Int J Mol Sci 2014,
15: 13615.
80. Allott EH, Howard LE, Cooperberg MR, Kane CJ, Aronson WJ, Terris MK,
Amling CL, Freedland SJ: Postoperatief statinegebruik en risico op biochemie
recidief na radicale prostatectomie: resultaten van de Shared
Gelijke toegang Regionaal Kankerziekenhuis (SEARCH) database. BJU Int 2014,
114: 661.
81. Jespersen CG, Norgaard M, Friis S, Skriver C, Borre M: gebruik van statines en risico op
prostaatkanker: een Deense populatie-gebaseerde case-control studie,
1997-2010. Kankerepidemie 2014, 38:42�47.
82. Meyers CD, Kashyap ML: farmacologische verhoging van hoge dichtheid
lipoproteïnen: recente inzichten over werkingsmechanisme en atherosclerose
bescherming. Curr Opin Cardiol 2004, 19:366�373.
83. Xia P, Vadas MA, Rye KA, Barter PJ, Gamble JR: lipoproteïnen met hoge dichtheid
(HDL) onderbreken de signaalroute van sfingosinekinase. Een mogelijke
mechanisme voor bescherming tegen atherosclerose door HDL. J Biol Chem
1999, 274:33143-33147.
84. Kotani K, Sekine Y, Ishikawa S, Ikpot IZ, Suzuki K, Remaley AT: Hoge dichtheid
lipoproteïne en prostaatkanker: een overzicht. J Epidemiol 2013,
23: 313.
85. Soni MG, Thurmond TS, Miller ER 3e, Spriggs T, Bendich A, Omaye ST:
Veiligheid van vitamines en mineralen: controverses en perspectief. Toxicol
Wetenschappelijk onderzoek 2010, 118:348-355.
86. Neuhouser ML, Barnett MJ, Kristal AR, Ambroson CB, King I, Thornquist M,
Goodman G: (n-6) PUFA-toename en zuivelproducten verlagen de prostaat
kankerrisico bij zware rokers. J Nutr 2007, 137:1821-1827.
87. Karppi J, Kurl S, Laukkanen JA, Kauhanen J: Serum beta-caroteen in relatie
risico op prostaatkanker: het Kuopio Ischemic Heart Disease Risk
Factor studie. Nutr Kanker 2012, 64:361�367.
88. Margalit DN, Kasperzyk JL, Martin NE, Sesso HD, Gaziano JM, Ma J, Stampfer
MJ, Mucci LA: gebruik van bètacaroteen-antioxidanten tijdens bestralingstherapie
en uitkomst van prostaatkanker in de Physicians' Health Study. Int J Radiat
Oncol Biol Phys 2012, 83:28-32.
89. Roswall N, Larsen SB, Friis S, Outzen M, Olsen A, Christensen J, Dragsted LO,
Tj�nneland A: Inname van micronutriënten en risico op prostaatkanker bij a
cohort Deense mannen van middelbare leeftijd. Kanker veroorzaakt controle 2013,
24: 1129.
90. Gilbert R, Metcalfe C, Fraser WD, Donovan J, Hamdy F, Neal DE, Lane JA,
Martin RM: Associaties van circulerend retinol, vitamine E en 1,25-
dihydroxyvitamine D met diagnose, stadium en graad van prostaatkanker.
Kanker veroorzaakt controle 2012, 23:1865�1873.
91. Bistulfi G, Foster BA, Karasik E, Gillard B, Miecznikowski J, Dhiman VK,
Smiraglia DJ: Foliumzuurdeficiëntie in de voeding blokkeert de progressie van prostaatkanker
in het TRAMP-model. Kanker Prev Res (Phila) 2011, 4:1825-1834.
92. Collin SM: foliumzuur en B12 bij prostaatkanker. Adv Clin Chem 2013,
60: 1.
93. Tio M, Andrici J, Cox MR, Eslick GD: inname van foliumzuur en het risico op prostaat
kanker: een systematische review en meta-analyse. Prostaatkanker Prostaat
Dis 2014, 17:213�219.
94. Vollset SE, Clarke R, Lewington S, Ebbing M, Halsey J, Lonn E, Armitage J,
Manson JE, Hankey GJ, Spence JD, Galan P, B�naa KH, Jamison R, Gaziano
JM, Guarino P, Baron JA, Logan RF, Giovannucci EL, den Heijer M, Ueland
PM, Bennett D, Collins R, Peto R, B-Vitamine Treatment Trialists' Samenwerking:
Effecten van foliumzuursuppletie op algehele en plaatsspecifieke kanker
incidentie tijdens de gerandomiseerde studies: meta-analyses van gegevens op 50,000
individuen. Lancet 2013, 381:1029-1036.
95. Verhage BA, Cremers P, Schouten LJ, Goldbohm RA, van den Brandt PA:
Dieet folaat en folaat vitamers en het risico op prostaatkanker
in de Nederlandse cohortstudie. Kanker veroorzaakt controle 2012,
23: 2003.
96. Tavani A, Malerba S, Pelucchi C, Dal Maso L, Zucchetto A, Serraino D, Levi F,
Montella M, Franceschi S, Zambon A, La Vecchia C: Folaten uit de voeding en
kankerrisico in een netwerk van case-control studies. Ann Oncol 2012,
23: 2737.
97. Moreira DM, Banez LL, Presti JC Jr, Aronson WJ, Terris MK, Kane CJ, Amling
CL, Freedland SJ: Hoog serumfolaat wordt geassocieerd met verlaagd
biochemisch recidief na radicale prostatectomie: resultaten van de
ZOEK Database. Int Braz J Urol 2013, 39:312�318. discussie 319.
98. Han YY, Song JY, Talbott EO: serumfoliumzuur en prostaatspecifiek antigeen in
de Verenigde Staten. Kanker veroorzaakt controle 2013, 24:1595�1604.
99. Rycyna KJ, Bacich DJ, O'Keefe DS: tegengestelde rollen van foliumzuur in de prostaat
kanker. Urologie 2013, 82:1197�1203.
100. Gilbert R, Martin RM, Beynon R, Harris R, Savovic J, Zuccolo L, Bekkering GE,
Fraser WD, Sterne JA, Metcalfe: Verenigingen van circulatie en voeding
vitamine D met risico op prostaatkanker: een systematische review en dosering�
respons meta-analyse. Kanker veroorzaakt controle 2011, 22:319�340.
101. Schenk JM, Tot CA, Tangen CM, Goodman PJ, Song X, Torkko KC, Kristal AR,
Peters U, Neuhouser ML: Serum 25-hydroxyvitamine D-concentraties en
risico op prostaatkanker: resultaten van de Prostate Cancer Prevention Trial.
Kanker Epidemiol Biomarkers Prev 2014, 23:1484�1493.
102. Schwartz GG: Vitamine D, in het bloed en risico op prostaatkanker: lessen
van de Selenium en Vitamine E Cancer Prevention Trial en de
Prostaat ter voorkoming van kanker. Kanker Epidemiol Biomarkers Vorige 2014,
23: 1447.
103. Giangreco AA, Vaishnav A, Wagner D, Finelli A, Fleshner N, Van der Kwast T,
Vieth R, Nonn L: Tumoronderdrukkende microRNA's, miR-100 en -125b, zijn
gereguleerd door 1,25-dihydroxyvitamine D in primaire prostaatcellen en in
weefsel van de patiënt. Kanker Prev Res (Phila) 2013, 6:483�494.
104. Hollis BW, Marshall DT, Savage SJ, Garrett-Mayer E, Kindy MS, Gattoni-Celli S:
Vitamine D3-suppletie, prostaatkanker met een laag risico en gezondheid
ongelijkheden. J Steroïde Biochem Mol Biol 2013, 136:233�237.
105. Sha J, Pan J, Ping P, Xuan H, Li D, Bo J, Liu D, Huang Y: synergetisch effect
en mechanisme van vitamine A en vitamine D bij het induceren van apoptose van
prostaat kankercellen. Mol Biol Rep 2013, 40:2763�2768.
106. Chandler PD, Giovannucci EL, Scott JB, Bennett GG, Ng K, Chan AT, Hollis
BW, Emmons KM, Fuchs CS, Drake BF: nulassociatie tussen vitamine D
en PSA-waarden bij zwarte mannen in een proef met vitamine D-suppletie.
Kanker Epidemiol Biomarkers Prev 2014, 23:1944�1947.
107. Skaaby T, Husemoen LL, Thuesen BH, Pisinger C, Jorgensen T, Roswall N,
Larsen SC, Linneberg A: Prospectieve populatie-gebaseerde studie van de
associatie tussen serum 25-hydroxyvitamine-D-spiegels en de
incidentie van specifieke soorten kanker. Kanker Epidemiol Biomarkers Vorige
2014, 23:1220-1229.
108. Holt SK, Kolb S, Fu R, Horst R, Feng Z, Stanford JL: circulerende niveaus van
25-hydroxyvitamine D en prostaatkankerprognose. Kanker Epidemiol
2013, 37:666-670.
109. Wong YY, Hyde Z, McCaul KA, Yeap BB, Golledge J, Hankey GJ, Flicker L:
Bij oudere mannen wordt een lager plasma 25-hydroxyvitamine D geassocieerd met
verminderde incidentie van prostaatkanker, maar niet van colorectale of longkanker.
PLoS One 2014, 9:e99954.
110. Xu Y, Shao X, Yao Y, Xu L, Chang L, Jiang Z, Lin Z: positieve associatie
tussen circulerende 25-hydroxyvitamine D-spiegels en het risico op prostaatkanker:
nieuwe bevindingen van een bijgewerkte meta-analyse. J Kanker Res Clin Oncol
2014, 140:1465-1477.
111. Meyer HE, Robsahm TE, Bjorge T, Brustad M, Blomhoff R: Vitamine D, seizoen,
en risico op prostaatkanker: een geneste case-control studie binnen
Noorse gezondheidsstudies. Am J Clin Nutr 2013, 97:147�154.
112. Kristal AR, Till C, Song X, Tangen CM, Goodman PJ, Neuhauser ML, Schenk
JM, Thompson IM, Meyskens FL Jr, Goodman GE, Minasian LM, Parnes HL,
Klein EA: Plasma vitamine D en risico op prostaatkanker: resultaten van de
Onderzoek naar kankerpreventie met selenium en vitamine E. Kanker Epidemiol
Biomarkers Vorige 2014, 23:1494�1504.
113. Weinstein SJ, Mondul AM, Kopp W, Rager H, Virtamo J, Albanes D:
Circulerend 25-hydroxyvitamine D, vitamine D-bindend eiwit en risico op
prostaatkanker. Int J Kreeft 2013, 132:2940�2947.
114. Guo Z, Wen J, Kan Q, Huang S, Liu X, Sun N, Li Z: gebrek aan associatie
tussen vitamine D-receptorgen FokI en BsmI-polymorfismen en risico op prostaatkanker: een bijgewerkte meta-analyse waarbij 21,756 proefpersonen betrokken waren. Tumor Biol 2013, 34:3189�3200115. Wang L, Sesso HD, Glynn RJ, Christen WG, Bubes V, Manson JE, Buring JE,
Gaziano JM: Suppletie van vitamine E en C en risico op kanker bij mannen:
posttriale follow-up in de Physicians' Health Study II gerandomiseerde trial.
Am J Clin Nutr 2014, 100: 915.
116. Virtamo J, Taylor PR, Kontto J, Mannisto S, Utriainen M, Weinstein SJ,
Huttunen J, Albanes D: effecten van alfa-tocoferol en bèta-caroteen
suppletie op kankerincidentie en mortaliteit: 18 jaar
follow-up na de interventie van het alfa-tocoferol, bèta-caroteen
Onderzoek naar kankerpreventie. Int J Kreeft 2014, 135:178�185.
117. Basu A, Imrhan V: vitamine E en prostaatkanker: is vitamine E-succinaat een
superieur chemopreventief middel? Nutr Rev 2005, 63:247-251.
118. Lawson KA, Wright ME, Subar A, Mouw T, Hollenbeck A, Schatzkin A,
Leitzmann MF: Multivitaminegebruik en risico op prostaatkanker in de
National Institutes of Health-AARP Diet and Health Study. J Natl Kanker
Inst 2007, 99:754-764.
119. Calle EE, Rodriguez C, Jacobs EJ, Almon ML, Chao A, McCullough ML,
Feigelson HS, Thun MJ: De American Cancer Society Kankerpreventie
Studie II Nutrition Cohort: grondgedachte, onderzoeksopzet en basislijn
kenmerken. Kanker 2002, 94:2490-2501.
120. Weinstein SJ, Peters U, Ahn J, Friesen MD, Riboli E, Hayes RB, Albanes D:
Serum alfa-tocoferol- en gamma-tocoferolconcentraties en
risico op prostaatkanker in de PLCO-screeningstudie: een geneste case-control
studie. PLoS One 2012, 7:e40204.
121. Cui R, Liu ZQ, Xu Q: bloed alfa-tocoferol, gamma-tocoferol niveaus
en risico op prostaatkanker: een meta-analyse van prospectieve studies.
PLoS One 2014, 9:e93044.
122. Majoor JM, Yu K, Weinstein SJ, Berndt SI, Hyland PL, Yeager M, Chanock S,
Albanes D: Genetische varianten die een hogere vitamine E-status bij mannen weerspiegelen, zijn dat wel
geassocieerd met een verminderd risico op prostaatkanker. J Nutr mei 2014,
144: 729.
123. Klein EA, Thompson IM Jr, Tangen CM, Crowley JJ, Lucia MS, Goodman PJ,
Minasian LM, Ford LG, Parnes HL, Gaziano JM, Karp DD, Lieber MM, Walther
PJ, Klotz L, Parsons JK, Chin JL, Darke AK, Lippman SM, Goodman GE,
Meyskens FL Jr, Baker LH: Vitamine E en het risico op prostaatkanker: de
Onderzoek naar kankerpreventie met selenium en vitamine E (SELECT). JAMA 2011,
306: 1549.
124. Albanes D, Till C, Klein EA, Goodman PJ, Mondul AM, Weinstein SJ, aylor PR,
Parnes HL, Gaziano JM, Song X, Fleshner NE, Brown PH, Meyskens FL Jr,
Thompson IM: Plasma-tocoferolen en risico op prostaatkanker in de
Onderzoek naar kankerpreventie met selenium en vitamine E (SELECT). Kanker Vorige res
(Phila) 2014, 7: 886-895.
125. Kristal AR, Darke AK, Morris JS, Tangen CM, Goodman PJ, Thompson IM,
Meyskens FL Jr, Goodman GE, Minasian LM, Parnes HL, Lippman SM,
Klein EA: Baseline seleniumstatus en effecten van selenium en vitamine e
suppletie op het risico op prostaatkanker. J Natl Kanker Inst 2014,
106: djt456.
126. Jamison JM, Gilloteaux J, Taper HS, Summers JL: Evaluatie van de in vitro
en in vivo antitumoractiviteiten van combinaties van vitamine C en K-3
tegen menselijke prostaatkanker. J Nutr 2001, 131:158S�160S.
127. Nimptsch K, Rohrmann S, Kaaks R, Linseisen J: vitamine K-inname via de voeding
met betrekking tot de incidentie en mortaliteit van kanker: resultaten van de
Heidelberg-cohort van het European Prospective Investigation into
Kanker en voeding (EPIC-Heidelberg). Ben J Clin Nutr 2010,
91: 1348.
128. Ma RW, Chapman K: een systematische review van het effect van voeding op de prostaat
preventie en behandeling van kanker. J Hum Nutr Dieet 2009, 22:187�199.
toets 200�182.
129. Bristow SM, Bolland MJ, MacLennan GS, Avenell A, Gray A, Gamble GD, Reid
IR: Calciumsupplementen en kankerrisico: een meta-analyse van gerandomiseerde
gecontroleerde proeven. Br J Nutr 2013, 110:1384�1393.
130. Williams CD, Whitley BM, Hoyo C, Grant DJ, Schwartz GG, Presti JC Jr, Iraggi
JD, Newman KA, Gerber L, Taylor LA, McKeever MG, Freedland SJ: Dieet
calcium en risico op prostaatkanker: een case-control studie onder de VS
veteranen. Vorige Chronische Dis 2012, 9:E39.
131. Hori S, Butler E, McLoughlin J: Prostaatkanker en voeding: stof tot nadenken?
BJU Int 2011, 107: 1348-1359.
132. Geybels MS, Verhage BA, van Schooten FJ, Goldbohm RA, van den Brandt
PA: Geavanceerd risico op prostaatkanker in relatie tot teennagelseleniumniveaus.
J Natl Cancer Inst 2013, 105: 1394-1401.
133. Singh RP, Agarwal R: Chemopreventie van prostaatkanker door silibinin: bank
naar bed. Mol Carcinog 2006, 45:436�442.
134. Ting H, Deep G, Agarwal R: moleculaire mechanismen van door silibinine gemedieerde
kankerchemopreventie met grote nadruk op prostaatkanker.
AAPS J 2013, 15:707-716.
135. Ting HJ, Deep G, Jain AK, Cimic A, Sirintrapun J, Romero LM, Cramer SD,
Agarwal C, Agarwal R: Silibinin voorkomt celgemedieerde prostaatkanker
differentiatie van naïeve fibroblasten in kanker-geassocieerde fibroblasten
fenotype door zich te richten op TGF beta2. Mol Kankerverwekkend 2014. doi:10.1002/
mc.22135. [Epub van tevoren]
136. Goel A, Aggarwal BB: Curcumine, het gouden kruid van Indiase saffraan, is een
chemosensitizer en radiosensitizer voor tumoren en chemoprotector en
radioprotector voor normale organen. Nutr Kanker 2010, 62:919�930.
137. Khan N, Adhami VM, Mukhtar H: apoptose door voedingsmiddelen voor
preventie en behandeling van prostaatkanker. Endocr Relat Kanker 2010,
17:R39�R52.
138. Heber D: Granaatappel ellagitanninen. In kruidengeneeskunde: biomoleculair en
Klinische aspecten. 2e editie. Bewerkt door Benzie IF, Wachtel-Galor S. Boca
Raton, Florida: CRC Pers; 2011.
139. Pantuck AJ, Leppert JT, Zomorodian N, Aronson W, Hong J, Barnard RJ,
Seeram N, Liker H, Wang H, Elashoff R, Heber D, Aviram M, Ignarro L,
Belldegrun A: Fase II studie van granaatappelsap voor mannen met rijzen
prostaatspecifiek antigeen na een operatie of bestraling voor de prostaat
kanker. Clin Cancer Res 2006, 12:4018�4026.
140. Paller CJ, Ye X, Wozniak PJ, Gillespie BK, Sieber PR, Greengold RH, Stockton
BR, Hertzman BL, Efros MD, Roper RP, Liker HR, Carducci MA: een gerandomiseerde
fase II studie van granaatappel extract voor mannen met stijgend PSA volgen
initiële therapie voor gelokaliseerde prostaatkanker. Prostaatkanker Prostaat Dis
2013, 16:50-55.
141. Freedland SJ, Carducci M, Kroeger N, Partin A, Rao JY, Jin Y, Kerkoutian S,
Wu H, Li Y, Creel P, Mundy K, Gurganus R, Fedor H, Koning SA, Zhang Y,
Heber D, Pantuck AJ: een dubbelblinde, gerandomiseerde, neoadjuvante studie van
de weefseleffecten van POMx-pillen bij mannen met prostaatkanker eerder
radicale prostatectomie. Kanker Prev Res (Phila) 2013, 6:1120�1127.
142. Wang P, Aronson WJ, Huang M, Zhang Y, Lee RP, Heber D, Henning SM:
Groene thee polyfenolen en metabolieten in prostatectomieweefsel:
implicaties voor de preventie van kanker. Kanker Prev Res (Phila) 2010,
3: 985.
143. Kurahashi N, Sasazuki S, Iwasaki M, Inoue M, Tsugane S: groene thee
consumptie en risico op prostaatkanker bij Japanse mannen: een prospectief
studie. Am J Epidemiol 2008, 167:71�77.
144. McLarty J, Bigelow RL, Smith M, Elmajian D, Ankem M, Cardelli JA: thee
polyfenolen verlagen de serumspiegels van prostaatspecifiek antigeen,
hepatocytgroeifactor en vasculaire endotheliale groeifactor
prostaatkankerpatiënten en remmen de productie van hepatocytengroei
factor en vasculaire endotheliale groeifactor in vitro. Kanker Vorige res
(Phila) 2009, 2: 673-682.
145. Bettuzzi S, Brausi M, Rizzi F, Castagnetti G, Peracchia G, Corti A:
Chemopreventie van prostaatkanker bij de mens door orale toediening van
catechines uit groene thee bij vrijwilligers met hoogwaardige intra-epitheliale prostaat
neoplasie: een voorlopig rapport van een eenjarig proof-of-principle-onderzoek.
Kankeronderzoek 2006, 66:1234-1240.
146. Fraser SP, Peters A, Fleming-Jones S, Mukhey D, Djamgoz MB: Resveratrol:
remmende effecten op gemetastaseerd celgedrag en voltage-gated Na (+)
kanaalactiviteit bij prostaatkanker bij ratten in vitro. Nutr Kanker 2014,
66: 1047.
147. Oskarsson A, Spatafora C, Tringali C, Andersson AO: remming van CYP17A1
activiteit door resveratrol, piceatannol en synthetische resveratrol-analogen.
Prostaat 2014, 74:839�851.
148. Ferruelo A, Romero I, Cabrera PM, Arance I, Andres G, Angulo JC: effecten van
resveratrol en andere wijnpolyfenolen op de proliferatie, apoptose
en androgeenreceptorexpressie in LNCaP-cellen. Actas Urol Esp jul-aug
2014, 38:397-404.
149. Osmond GW, Masko EM, Tyler DS, Freedland SJ, Pizzo S: In vitro en in vivo
evaluatie van resveratrol en 3,5-dihydroxy-4β-acetoxy-trans-stilbeen in
de behandeling van humaan prostaatcarcinoom en melanoom. J Surg Res
2013, 179: e141�e148.
150. Baur JA, Sinclair DA: Therapeutisch potentieel van resveratrol: de in vivo
bewijs. Nat Rev Drug Discov 2006, 5:493�506.
151. Klink JC, Tewari AK, Masko EM, Antonelli J, Febbo PG, Cohen P, Dewhirst
MW, Pizzo SV, Freedland SJ: Resveratrol verslechtert de overleving bij SCID-muizen met xenotransplantaten van prostaatkanker op een cellijnspecifieke manier, door paradoxale effecten op oncogene routes. Prostaat 2013, 73:754�762.
152. Huang EC, Zhao Y, Chen G, Baek SJ, McEntee MF, Minkin S, Biggerstaff JP,
Whelan J: Zyflamend, een polykruidenmengsel, reguleert klasse I en down
klasse II histon deacetylasen en verhoogt p21-niveaus in castratieresistent
prostaat kankercellen. BMC Complement Altern Med 2014, 14:68.
153. Huang EC, McEntee MF, Whelan J: Zyflamend, een combinatie van kruiden
extracten, remt tumorgroei in muriene xenotransplantaatmodellen van
prostaatkanker. Nutr Kanker 2012, 64:749�760.
154. Yan J, Xie B, Capodice JL, Katz AE: Zyflamend remt de expressie en
functie van de androgeenreceptor en werkt synergetisch met bicalutimide
om de groei van prostaatkankercellen te remmen. Prostaat 2012, 72:244�252.
155. Kunnumakkara AB, Sung B, Ravindran J, Diagaradjane P, Deorukhkar A, Dey
S, Koca C, Tong Z, Gelovani JG, Guha S, Krishnan S, Aggarwal BB: Zyflamend
onderdrukt de groei en maakt menselijke alvleeskliertumoren gevoelig voor
gemcitabine in een orthotopisch muismodel door modulatie van
meerdere doelen. Int J Kanker 2012, 131:E292�E303.
156. Capodice JL, Gorroochurn P, Cammack AS, Eric G, McKiernan JM, Benson
MC, Stone BA, Katz AE: Zyflamend bij mannen met hoogwaardige prostaat
intra-epitheliale neoplasie: resultaten van een fase I klinische studie. J Soc Integr
Oncol 2009, 7:43-51.
157. Rafailov S, Cammack S, Stone BA, Katz AE: de rol van Zyflamend, een
kruiden ontstekingsremmend, als een potentieel chemopreventief middel tegen
prostaatkanker: een casusrapport. Integr Cancer Ther 2007, 6:74�76.
158. Askari F, Parizi MK, Jessri M, Rashidkhani B: inname van groenten en fruit in
relatie met prostaatkanker bij Iraanse mannen: een case-control studie.
Aziatische Pac J Kanker Vorige 2014, 15:5223�5227.
159. Liu B, Mao Q, Cao M, Xie L: inname van kruisbloemige groenten en risico op
prostaatkanker: een meta-analyse. Int J Urol 2012, 19:134�141.
160. Richman EL, Carroll PR, Chan JM: inname van groenten en fruit daarna
diagnose en risico op progressie van prostaatkanker. Int J Kreeft 2012,
131: 201.
161. Hsing AW, Chokkalingam AP, Gao YT, Madigan MP, Deng J, Gridley G,
Fraumeni JF Jr.: Alliumgroenten en risico op prostaatkanker: een
bevolkingsonderzoek. J Natl Cancer Inst. 2002, 94:1648-1651.
162. Chan R, Lok K, Woo J: Prostaatkanker en groenteconsumptie.
Mol Nutr Food Res 2009, 53:201-216.
163. Thomas R, Williams M, Sharma H, Chaudry A, Bellamy P: een dubbelblinde,
placebogecontroleerde gerandomiseerde studie die het effect evalueerde van a
polyfenolrijk volwaardig voedingssupplement over PSA-progressie bij mannen
met prostaatkanker - de Britse NCRN Pomi-T-studie. Prostaatkanker Prostaat
Dis 2014, 17:180�186.
164. Yang CM, Lu IH, Chen HY, Hu ML: Lycopeen remt de proliferatie van
androgeenafhankelijke humane prostaattumorcellen door activatie van
PPARgamma-LXRalpha-ABCA1-route. J Nutr Biochem 2012, 23:8�17.
165. Qiu X, Yuan Y, Vaishnav A, Tessel MA, Nonn L, van Breemen RB: effecten van
lycopeen op eiwitexpressie in menselijk primair prostaatepitheel
cellen. Kanker Prev Res (Phila) 2013, 6:419�427.
166. Boileau TW, Liao Z, Kim S, Lemeshow S, Erdman JW Jr, Clinton SK: Prostaat
carcinogenese in N-methyl-N-nitrosourea (NMU)-testosteron-behandeld
ratten kregen tomatenpoeder, lycopeen of energiebeperkte diëten. J Natl
Kanker Inst. 2003, 95:1578-1586.
167. Konijeti R, Henning S, Moro A, Sheikh A, Elashoff D, Shapiro A, Ku M,
Said JW, Heber D, Cohen P, Aronson WJ: Chemopreventie van prostaat
kanker met lycopeen in het TRAMP-model. Prostaat 2010, 70:1547�1554.
168. Giovannucci E, Rimm EB, Liu Y, Stampfer MJ, Willett WC: een toekomstige
studie van tomatenproducten, lycopeen en risico op prostaatkanker. J Natl
Kanker Inst. 2002, 94:391-398.
169. Zu K, Mucci L, Rosner BA, Clinton SK, Loda M, Stampfer MJ, Giovannucci E:
Dieet lycopeen, angiogenese en prostaatkanker: een prospectief
studie in het prostaatspecifieke antigeentijdperk. J Natl Kanker Inst 2014,
106: djt430.
170. Gann PH, Ma J, Giovannucci E, Willett W, Sacks FM, Hennekens CH, Stampfer
MJ: lager risico op prostaatkanker bij mannen met verhoogd plasma-lycopeen
niveaus: resultaten van een prospectieve analyse. Kankeronderzoek 1999, 59:1225-1230.
171. Kristal AR, Till C, Platz EA, Song X, King IB, Neuhouser ML, Ambroson CB,
Thompson IM: serumlycopeenconcentratie en risico op prostaatkanker:
resultaten van de Prostate Cancer Prevention Trial. Kanker Epidemiol
Biomarkers Vorige 2011, 20:638�646.
172. Kirsh VA, Mayne ST, Peters U, Chatterjee N, Leitzmann MF, Dixon LB, Stedelijk
DA, Crawford ED, Hayes RB: een prospectieve studie van lycopeen en tomaat
productinname en risico op prostaatkanker. Kanker Epidemiol Biomarkers
Vorige 2006, 15:92�98.
173. Mariani S, Lionetto L, Cavallari M, Tubaro A, Rasio D, De Nunzio C, Hong
GM, Borro M, Simmaco M: Lage prostaatconcentratie van lycopeen is
geassocieerd met de ontwikkeling van prostaatkanker bij patiënten met een hoge graad
prostaat intra-epitheliale neoplasie. Int J Mol Sci 2014, 15:1433�1440.
174. Kucuk O, Sarkar FH, Djuric Z, Sakr W, Pollak MN, Khachik F, Banerjee M,
Bertram JS, Wood DP Jr: effecten van lycopeensuppletie bij patiënten
met gelokaliseerde prostaatkanker. Exp Biol Med (Maywood) 2002, 227:881-885.
175. Chen L, Stacewicz-Sapuntzakis M, Duncan C, Sharifi R, Ghosh L, van
Breemen R, Ashton D, Bowen PE: oxidatieve DNA-schade in de prostaat
kankerpatiënten die voorgerechten op basis van tomatensaus consumeren als volwaardig voedsel
interventie. J Natl Cancer Inst. 2001, 93:1872-1879.
176. van Breemen RB, Sharifi R, Viana M, Pajkovic N, Zhu D, Yuan L, Yang Y,
Bowen PE, Stacewicz-Sapuntzakis M: antioxiderende effecten van lycopeen in
Afro-Amerikaanse mannen met prostaatkanker of goedaardige prostaathyperplasie:
een gerandomiseerde, gecontroleerde studie. Kanker Prev Res (Phila) 2011, 4:711-718.
177. Shafique K, McLoone P, Qureshi K, Leung H, Hart C, Morrison DS: Koffie
consumptie en risico op prostaatkanker: verder bewijs voor omgekeerd
relatie. Nutr J 2012, 11:42.
178. Wilson KM, Kasperzyk JL, Rider JR, Kenfield S, van Dam RM, Stampfer MJ,
Giovannucci E, Mucci LA: koffieconsumptie en risico op prostaatkanker
en progressie in de Health Professionals Follow-up Study. J Natl
Kanker Inst. 2011, 103:876-884.
179. Bosire C, Stampfer MJ, Subar AF, Wilson KM, Park Y, Sinha R: koffie
consumptie en het risico van algemene en dodelijke prostate kanker in
NIH-AARP dieet- en gezondheidsstudie. Kanker veroorzaakt controle 2013, 24:1527�1534.
180. Arab L, Su LJ, Steck SE, Ang A, Fontham ET, Bensen JT, Mohler JL: koffie
consumptie en prostate kankeragressiviteit onder Afrikaan en
Blanke Amerikanen in een populatieonderzoek. Nutr Kanker 2012,
64: 637.
181. Phillips RL, Snowdon DA: associatie van vlees- en koffiegebruik met kanker
van de dikke darm, borst en prostaat onder Zevende-dags Adventisten:
voorlopige resultaten. Cancer Res 1983, 43:2403 s�2408s.
182. Hsing AW, McLaughlin JK, Schuman LM, Bjelke E, Gridley G, Wacholder S,
Chien HT, Blot WJ: Dieet, tabaksgebruik en dodelijke prostaatkanker: resultaten
van de Lutheran Brotherhood Cohort Study. Kankeronderzoek 1990,
50: 6836.
183. Cao S, Liu L, Yin X, Wang Y, Liu J, Lu Z: koffieconsumptie en risico op
prostaatkanker: een meta-analyse van prospectieve cohortstudies.
Kankerverwekkendheid 2014, 35:256-261.
184. Nordmann AJ, Suter-Zimmermann K, Bucher HC, Shai I, Tuttle KR,
Estruch R, Briel M: meta-analyse waarin mediterraan wordt vergeleken met vetarm
diëten voor wijziging van cardiovasculaire risicofactoren. Ben J Med 2011,
124:841-851. e842.
185. Kapiszewska M: Een groente-vleesconsumptieverhouding als relevant
factor die kankerpreventief dieet bepaalt. De Middellandse Zee versus
andere Europese landen. Forum Nutr 2006, 59:130�153.
186. Kenfield SA, Dupre N, Richman EL, Stampfer MJ, Chan JM, Giovannucci EL:
Mediterraan dieet en risico op prostaatkanker en mortaliteit in de gezondheid
Beroepsvervolgonderzoek. Eur Urol 2014, 65:887�894.
187. Ambrosini GL, Fritschi L, de Klerk NH, Mackerras D, Leavy J: voedingspatronen
geïdentificeerd met behulp van factoranalyse en prostaatkankerrisico: een casuscontrole
studeren in West-Australië. Ann Epidemiol 2008, 18:364�370.
188. Baade PD, Youlden DR, Krnjacki LJ: Internationale epidemiologie van prostaat
kanker: geografische spreiding en seculiere trends. Mol Nutr Food Res
2009, 53:171-184.
189. Muller DC, Severi G, Baglietto L, Krishnan K, Engelse DR, Hopper JL, Giles GG:
Dieetpatronen en risico op prostaatkanker. Kanker Epidemiol Biomarkers Vorige
2009, 18:3126-3129.
190. Tseng M, Breslow RA, DeVellis RF, Ziegler RG: voedingspatronen en prostaat
kankerrisico in de National Health and Nutrition Examination Survey
Epidemiologische vervolgonderzoekscohort. Kanker Epidemiol Biomarkers Vorige
2004, 13:71-77.
191. Wu K, Hu FB, Willett WC, Giovannucci E: voedingspatronen en risico op
prostaatkanker bij Amerikaanse mannen. Kanker Epidemiol Biomarkers Prev 2006,
15: 167.
192. Daubenmier JJ, Weidner G, Marlin R, Crutchfield L, Dunn-Emke S, Chi C,
Gao B, Carroll P, Ornish D: levensstijl en gezondheidsgerelateerde levenskwaliteit van
mannen met prostaatkanker beheerd met actief toezicht. Urologie
2006, 67:125-130.
193. Parsons JK, Newman VA, Mohler JL, Pierce JP, Flatt S, Marshall J: Dieet
modificatie bij patiënten met prostaatkanker op actief toezicht:
gerandomiseerde, multicenter haalbaarheidsstudie. BJU Int 2008, 101:1227�1231.
194. Mosher CE, Sloane R, Morey MC, Snyder DC, Cohen HJ, Miller PE,
Demark-Wahnefried W: Associaties tussen leefstijlfactoren en kwaliteit
van het leven onder oudere langdurige borst-, prostaat- en colorectale kanker
overlevenden. Kreeft 2009, 115:4001-4009.
195. Bhindi B, Locke J, Alibhai SM, Kulkarni GS, Margel DS, Hamilton RJ, Finelli A,
Trachtenberg J, Zlotta AR, Toi A, Hersey KM, Evans A, van der Kwast TH,
Fleshner NE: Ontleden van de associatie tussen metabool syndroom
en het risico op prostaatkanker: analyse van een groot klinisch cohort. Euro Urol 2014.
doi:10.1016/j.eururo.2014.01.040. [Epub van tevoren]
196. Esposito K, Chiodini P, Capuano A, Bellastella G, Maiorino MI, Parretta E,
Lenzi A, Giugliano D: Effect van metabool syndroom en zijn componenten
over het risico op prostaatkanker: meta-analyse. J Endocrinol Invest 2013,
36: 132.
197. Amerikaanse ministerie van Landbouw en Amerikaanse ministerie van Volksgezondheid en
Menselijke diensten. Dieetrichtlijnen voor Amerikanen, 2010. 7e editie.
Washington, DC: drukkerij van de Amerikaanse overheid, december 2010.
Accordeon sluiten
Professionele reikwijdte van de praktijk *
De informatie hierin over "Prostaatkanker, voeding en dieetinterventies" is niet bedoeld ter vervanging van een een-op-een relatie met een gekwalificeerde zorgverlener of gediplomeerde arts en is geen medisch advies. We moedigen u aan om beslissingen over de gezondheidszorg te nemen op basis van uw onderzoek en samenwerking met een gekwalificeerde zorgverlener.
Blog Informatie & Scope Discussies
Ons informatiebereik: is beperkt tot chiropractie, musculoskeletale, fysieke medicijnen, welzijn, bijdragende etiologische viscerosomatische stoornissen binnen klinische presentaties, geassocieerde somatoviscerale reflex klinische dynamiek, subluxatiecomplexen, gevoelige gezondheidskwesties en/of functionele geneeskunde artikelen, onderwerpen en discussies.
Wij bieden en presenteren klinische samenwerking met specialisten uit verschillende disciplines. Elke specialist wordt beheerst door hun professionele praktijk en hun jurisdictie van licentiestatus. We gebruiken functionele gezondheids- en welzijnsprotocollen om de verwondingen of aandoeningen van het bewegingsapparaat te behandelen en te ondersteunen.
Onze video's, berichten, onderwerpen, onderwerpen en inzichten behandelen klinische zaken, problemen en onderwerpen die verband houden met en direct of indirect onze klinische praktijk ondersteunen.*
Ons kantoor heeft redelijkerwijs geprobeerd om ondersteunende citaten te geven en heeft de relevante onderzoeksstudie of studies geïdentificeerd die onze berichten ondersteunen. Wij verstrekken kopieën van ondersteunende onderzoeksstudies die op verzoek beschikbaar zijn voor regelgevende instanties en het publiek.
We begrijpen dat we zaken behandelen die een aanvullende uitleg vereisen over hoe het kan helpen bij een bepaald zorgplan of behandelprotocol; daarom, om het onderwerp hierboven verder te bespreken, aarzel dan niet om te vragen Dr. Alex Jimenez, DC, of neem contact met ons op 915-850-0900.
Wij zijn er om u en uw gezin te helpen.
zegeningen
Dr. Alex Jimenez DC MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
e-mail: coach@elpasofunctionalmedicine.com
Licentie als Doctor of Chiropractic (DC) in Texas & New Mexico*
Texas DC-licentie # TX5807, New Mexico DC-licentie # NM-DC2182
Licentie als geregistreerde verpleegkundige (RN*) in Florida
Florida-licentie RN-licentie # RN9617241 (controle nr. 3558029)
Compacte status: Licentie voor meerdere staten: Geautoriseerd om te oefenen in 40 Staten*
Dr. Alex Jimenez DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Mijn digitale visitekaartje






