Pijn is de natuurlijke reactie van het menselijk lichaam op verwonding of ziekte, en het is vaak een waarschuwing dat er iets mis is. Zodra het probleem is genezen, hebben we over het algemeen geen last meer van deze pijnlijke symptomen, maar wat gebeurt er als de pijn aanhoudt lang nadat de oorzaak is verdwenen? Chronische pijn wordt medisch gedefinieerd als aanhoudende pijn die 3 tot 6 maanden of langer aanhoudt. Chronische pijn is zeker een uitdagende aandoening om mee te leven, die van invloed is op alles, van het individuele activiteitenniveau en hun vermogen om te werken, evenals hun persoonlijke relaties en psychologische omstandigheden. Maar weet u dat chronische pijn ook de structuur en functie van uw hersenen kan beïnvloeden? Het blijkt dat deze hersenveranderingen kunnen leiden tot zowel cognitieve als psychologische stoornissen.
Chronische pijn beïnvloedt niet alleen een enkelvoudig deel van de geest, het kan zelfs leiden tot veranderingen in tal van essentiële hersengebieden, waarvan de meeste betrokken zijn bij veel fundamentele processen en functies. Verschillende onderzoeken door de jaren heen hebben veranderingen in de hippocampus gevonden, samen met vermindering van grijze stof van de dorsolaterale prefrontale cortex, amygdala, hersenstam en rechter insulaire cortex, om er maar een paar te noemen, geassocieerd met chronische pijn. Een uitsplitsing van enkele van de structuur van deze regio's en hun gerelateerde functies kan helpen om deze hersenveranderingen in de juiste context te plaatsen, voor veel mensen met chronische pijn. Het doel van het volgende artikel is om de structurele en functionele hersenveranderingen die gepaard gaan met chronische pijn aan te tonen en te bespreken, met name in het geval dat deze waarschijnlijk geen schade of atrofie weerspiegelen.
Inhoud
Structurele hersenveranderingen bij chronische pijn weerspiegelen waarschijnlijk noch schade, noch atrofie
Abstract
Chronische pijn lijkt geassocieerd te zijn met vermindering van grijze stof in de hersenen in gebieden die kunnen worden toegeschreven aan de overdracht van pijn. De morfologische processen die ten grondslag liggen aan deze structurele veranderingen, waarschijnlijk na functionele reorganisatie en centrale plasticiteit in de hersenen, blijven onduidelijk. De pijn bij artrose van de heup is een van de weinige chronische pijnsyndromen die in principe te genezen zijn. We onderzochten 20 patiënten met chronische pijn als gevolg van unilaterale coxartrose (gemiddelde leeftijd 63.25-9.46 (SD) jaar, 10 vrouwen) vóór endoprothesechirurgie van het heupgewricht (pijntoestand) en volgden structurele veranderingen in de hersenen tot 1 jaar na de operatie: 6 weken , 8 weken en 12 maanden wanneer volledig pijnvrij. Patiënten met chronische pijn als gevolg van unilaterale coxartrose hadden significant minder grijze stof in vergelijking met controles in de anterieure cingulate cortex (ACC), insulaire cortex en operculum, dorsolaterale prefrontale cortex (DLPFC) en orbitofrontale cortex. Deze regio's functioneren als multi-integratieve structuren tijdens het ervaren van en het anticiperen op pijn. Toen de patiënten pijnvrij waren na herstel van endoprothetische chirurgie, werd een toename van de grijze stof in bijna dezelfde gebieden gevonden. We vonden ook een progressieve toename van grijze hersenstof in de premotorische cortex en het supplementaire motorgebied (SMA). We concluderen dat afwijkingen in de grijze stof bij chronische pijn niet de oorzaak, maar secundair zijn aan de ziekte en ten minste gedeeltelijk te wijten zijn aan veranderingen in motorische functie en lichamelijke integratie.
Introductie
Bewijs van functionele en structurele reorganisatie bij chronische pijnpatiënten ondersteunt het idee dat chronische pijn niet alleen moet worden geconceptualiseerd als een veranderde functionele toestand, maar ook als een gevolg van functionele en structurele hersenplasticiteit [1], [2], [3], [4], [5], [6]. In de afgelopen zes jaar zijn er meer dan 20 onderzoeken gepubliceerd die structurele hersenveranderingen aantonen bij 14 chronische pijnsyndromen. Een opvallend kenmerk van al deze onderzoeken is het feit dat de veranderingen in de grijze stof niet willekeurig werden verdeeld, maar optreden in gedefinieerde en functioneel zeer specifieke hersengebieden, namelijk betrokkenheid bij supraspinale nociceptieve verwerking. De meest opvallende bevindingen waren verschillend voor elk pijnsyndroom, maar overlapten elkaar in de cingulate cortex, de orbitofrontale cortex, de insula en de dorsale pons [4]. Verdere structuren omvatten de thalamus, de dorsolaterale prefrontale cortex, de basale ganglia en het hippocampale gebied. Deze bevindingen worden vaak besproken als cellulaire atrofie, wat het idee van schade of verlies van grijze hersenstof versterkt [7], [8], [9]. In feite vonden onderzoekers een correlatie tussen afname van grijze stof in de hersenen en duur van pijn [6], [10]. Maar de duur van pijn is ook gekoppeld aan de leeftijd van de patiënt, en de leeftijdsafhankelijke wereldwijde, maar ook regionaal specifieke afname van grijze stof is goed gedocumenteerd [11]. Aan de andere kant kunnen deze structurele veranderingen ook een afname zijn in celgrootte, extracellulaire vloeistoffen, synaptogenese, angiogenese of zelfs als gevolg van veranderingen in het bloedvolume [4], [12], [13]. Wat de bron ook is, voor onze interpretatie van dergelijke bevindingen is het belangrijk om deze morfometrische bevindingen te zien in het licht van een schat aan morfometrische onderzoeken naar inspanningsafhankelijke plasticiteit, aangezien regionaal specifieke structurele hersenveranderingen herhaaldelijk zijn aangetoond na cognitieve en fysieke inspanning [ 14].
Het is niet duidelijk waarom slechts een relatief klein deel van de mensen een chronisch pijnsyndroom ontwikkelt, aangezien pijn een universele ervaring is. De vraag rijst of bij sommige mensen een structureel verschil in centrale pijnoverdrachtsystemen kan werken als een diathese voor chronische pijn. Grijze stofveranderingen in fantoompijn als gevolg van amputatie [15] en ruggenmergletsel [3] geven aan dat de morfologische veranderingen van de hersenen, althans gedeeltelijk, een gevolg zijn van chronische pijn. De pijn bij heupartrose (OA) is echter een van de weinige chronische pijnsyndroom dat in principe te genezen is, aangezien 88% van deze patiënten regelmatig pijnvrij is na een totale heupprothese (THR) [16]. In een pilotstudie hebben we tien patiënten met heupartrose voor en kort na de operatie geanalyseerd. We vonden afname van grijze stof in de anterior cingulated cortex (ACC) en insula tijdens chronische pijn vóór THR-chirurgie en vonden toename van grijze stof in de corresponderende hersengebieden in de pijnvrije toestand na de operatie [17]. Door ons op dit resultaat te concentreren, hebben we nu onze onderzoeken uitgebreid naar meer patiënten (n?=?20) na succesvolle THR en hebben we structurele hersenveranderingen gevolgd in vier tijdsintervallen, tot een jaar na de operatie. Om te controleren op veranderingen in grijze stof als gevolg van motorische verbetering of depressie, hebben we ook vragenlijsten afgenomen die gericht waren op verbetering van motorische functie en mentale gezondheid.
Materialen en methoden
Vrijwilligers
De hier gerapporteerde patiënten zijn een subgroep van 20 patiënten van de 32 recent gepubliceerde patiënten die werden vergeleken met een gezonde controlegroep op basis van leeftijd en geslacht [17] maar deelnamen aan een aanvullend follow-uponderzoek van een jaar. Na de operatie vielen 12 patiënten af vanwege een tweede endoprothese (n?=?2), ernstige ziekte (n?=?2) en intrekking van de toestemming (n?=?8). Dit liet een groep van twintig patiënten over met unilaterale primaire heupartrose (gemiddelde leeftijd 63.25 (SD) jaar, 9.46 vrouwen) die vier keer werden onderzocht: vóór de operatie (pijntoestand) en opnieuw 10 en 6 weken en 8 �12 maanden na endoprothetische chirurgie, wanneer volledig pijnvrij. Alle patiënten met primaire heupartrose hadden een voorgeschiedenis van pijn langer dan 18 maanden, variërend van 10 tot 14 jaar (gemiddeld 12 jaar) en een gemiddelde pijnscore van 1 (variërend van 33 tot 7.35) op een visueel analoge schaal (VAS) variërend van 65.5 (geen pijn) tot 40 (ergst denkbare pijn). We beoordeelden elk optreden van kleine pijngebeurtenissen, waaronder tand-, oor- en hoofdpijn tot 90 weken voorafgaand aan het onderzoek. We selecteerden ook willekeurig de gegevens van 0 gezonde controles op geslacht en leeftijd (gemiddelde leeftijd 100-4 (SD) jaar, 20 vrouwen) van de 60,95 van de bovengenoemde pilotstudie [8,52]. Geen van de 10 patiënten of van de 32 gezonde vrijwilligers die qua geslacht en leeftijd overeenkwamen, had een neurologische of interne medische voorgeschiedenis. De studie kreeg ethische goedkeuring van de lokale ethische commissie en voorafgaand aan het onderzoek werd schriftelijke geïnformeerde toestemming verkregen van alle deelnemers aan de studie.
Gedragsgegevens
We verzamelden gegevens over depressie, somatisatie, angst, pijn en fysieke en mentale gezondheid bij alle patiënten en alle vier de tijdstippen met behulp van de volgende gestandaardiseerde vragenlijsten: Beck Depression Inventory (BDI) [18], Brief Symptom Inventory (BSI) [19], Schmerzempfindungs-Skala (SES?=?pijnonaangenaamheidsschaal) [20] en Health Survey 36-Item Short Form (SF-36) [21] en het Nottingham Health Profile (NHP). We voerden ANOVA met herhaalde metingen uit en koppelden tweezijdige t-Tests om de longitudinale gedragsgegevens te analyseren met behulp van SPSS 13.0 voor Windows (SPSS Inc., Chicago, IL), en gebruikten Greenhouse Geisser-correctie als de aanname voor bolvormigheid werd geschonden. Het significantieniveau werd ingesteld op p<0.05.
VBM – Data-acquisitie
Afbeeldingen verwerving. MR-scanning met hoge resolutie werd uitgevoerd op een 3T MRI-systeem (Siemens Trio) met een standaard 12-kanaals hoofdspoel. Voor elk van de vier tijdstippen, scan I (tussen 1 dag en 3 maand vóór endoprothetische chirurgie), scan II (6 tot 8 weken na de operatie), scan III (12 tot 18 weken na de operatie) en scan IV (10 maanden na de operatie) werd voor elke patiënt een T14-gewogen structurele MRI verkregen met behulp van een 1D-FLASH-sequentie (TR 3 ms, TE 15 ms, kantelhoek 4.9�, plakjes van 25 mm, FOV 1�256, voxelgrootte 256�1� 1mm).
Beeldverwerking en statistische analyse
Voorbewerking en analyse van gegevens werden uitgevoerd met SPM2 (Wellcome Department of Cognitive Neurology, Londen, VK) die onder Matlab (Mathworks, Sherborn, MA, VS) liep en een op voxel gebaseerde morfometrie (VBM)-toolbox voor longitudinale gegevens bevat, die is gebaseerd op structurele 3D MR-beelden met hoge resolutie en maakt het mogelijk om voxelgewijze statistieken toe te passen om regionale verschillen in dichtheid of volumes van grijze stof te detecteren [22], [23]. Samenvattend omvatte voorbewerking ruimtelijke normalisatie, segmentatie van grijze materie en 10 mm ruimtelijke afvlakking met een Gauss-kernel. Voor de voorbewerkingsstappen gebruikten we een geoptimaliseerd protocol [22], [23] en een scanner- en studiespecifieke grijze-stofsjabloon [17]. We gebruikten SPM2 in plaats van SPM5 of SPM8 om deze analyse vergelijkbaar te maken met onze pilotstudie [17]. omdat het een uitstekende normalisatie en segmentatie van longitudinale gegevens mogelijk maakt. Echter, aangezien een recentere update van VBM (VBM8) onlangs beschikbaar kwam (dbm.neuro.uni-jena.de/vbm/), gebruikten we ook VBM8.
Transversale analyse
We gebruikten een t-test met twee steekproeven om regionale verschillen in grijze hersenstof tussen groepen te detecteren (patiënten op tijdpuntscan I (chronische pijn) en gezonde controles). We hebben een drempel van p<0.001 (ongecorrigeerd) toegepast op de hele hersenen vanwege onze sterke a-priorische hypothese, die is gebaseerd op 9 onafhankelijke onderzoeken en cohorten die een afname van de grijze stof bij chronische pijnpatiënten laten zien [7], [8], [ 9], [15], [24], [25], [26], [27], [28], dat toename van grijze stof in dezelfde (voor pijnverwerking relevante) regio's zal verschijnen als in onze pilotstudie (17 ). De groepen waren gematcht voor leeftijd en geslacht zonder significante verschillen tussen de groepen. Om te onderzoeken of de verschillen tussen groepen na een jaar veranderden, vergeleken we ook patiënten op tijdstip scan IV (pijnvrij, een jaar follow-up) met onze gezonde controlegroep.
Longitudinale analyse
Om verschillen tussen tijdstippen (Scan I�IV) te detecteren, vergeleken we de scans vóór de operatie (pijntoestand) en opnieuw 6 en 8 weken en 12 maanden na endoprothetische chirurgie (pijnvrij) als ANOVA met herhaalde metingen. Omdat eventuele hersenveranderingen als gevolg van chronische pijn enige tijd nodig hebben om te verdwijnen na de operatie en het stoppen van de pijn en vanwege de pijn na de operatie die de patiënten rapporteerden, vergeleken we in de longitudinale analyse scan I en II met scan III en IV. Voor het detecteren van veranderingen die niet nauw verband houden met pijn, hebben we ook gezocht naar progressieve veranderingen over alle tijdsintervallen. We hebben de hersenen van patiënten met artrose van de linkerheup omgedraaid (n?=?18) om te normaliseren voor de zijde van de pijn voor beide, de groepsvergelijking en de longitudinale analyse, maar analyseerden voornamelijk de niet-gespiegelde gegevens. We gebruikten de BDI-score als covariabele in het model.
Resultaten
Gedragsgegevens
Alle patiënten meldden chronische heuppijn voor de operatie en waren pijnvrij (met betrekking tot deze chronische pijn) onmiddellijk na de operatie, maar rapporteerden vrij acute pijn na de operatie op scan II die anders was dan de pijn als gevolg van artrose. De mentale gezondheidsscore van de SF-36 (F(1.925/17.322)?=?0.352, p?=?0.7) en de BSI globale score GSI (F(1.706/27.302)?=?3.189, p?=?0.064 ) vertoonden geen veranderingen in het tijdsverloop en geen mentale comorbiditeit. Geen van de controles rapporteerde enige acute of chronische pijn en geen enkele vertoonde symptomen van depressie of lichamelijke/mentale handicap.
Vóór de operatie vertoonden sommige patiënten milde tot matige depressieve symptomen in BDI-scores die significant afnamen op scan III (t(17)?=?2.317, p?=?0.033) en IV (t(16)?=?2.132, p? =?0.049). Bovendien verbeterden de SES-scores (onaangename pijn) van alle patiënten significant van scan I (vóór de operatie) tot scan II (t(16)?=?4.676, p<0.001), scan III (t(14)?=? 4.760, p<0.001) en scan IV (t(14)?=?4.981, p<0.001, 1 jaar na de operatie) omdat de onaangename pijn afnam met de intensiteit van de pijn. De pijnscore op scan 1 en 2 was positief, dezelfde score op dag 3 en 4 negatief. De SES beschrijft alleen de kwaliteit van ervaren pijn. Het was daarom positief op dag 1 en 2 (gemiddeld 19.6 op dag 1 en 13.5 op dag 2) en negatief (nvt) op dag 3 & 4. Sommige patiënten begrepen deze procedure echter niet en gebruikten de SES als een globale kwaliteit levensmaat. Dit is de reden waarom alle patiënten op dezelfde dag individueel en door dezelfde persoon werden gevraagd naar het optreden van pijn.
In de korte gezondheidsenquête (SF-36), die bestaat uit de samenvattende maatregelen van een fysieke gezondheidsscore en een geestelijke gezondheidsscore [29], verbeterden de patiënten significant in de fysieke gezondheidsscore van scan I tot scan II (t( 17)?=??4.266, p?=?0.001), scan III (t(16)?=??8.584, p<0.001) en IV (t(12)?=??7.148, p<0.001), maar niet in de Mental Health Score. De resultaten van de NHP waren vergelijkbaar, in de subschaal 'pijn' (omgekeerde polariteit) zagen we een significante verandering van scan I naar scan II (t(14)?=??5.674, p<0.001, scan III (t(12 )?=??7.040, p<0.001 en scan IV (t(10)?=??3.258, p?=?0.009) We vonden ook een significante toename in de subschaal �fysieke mobiliteit� van scan I naar scan III (t(12)?=??3.974, p?=?0.002) en scan IV (t(10)?=??2.511, p?=?0.031) Er was geen significante verandering tussen scan I en scan II ( zes weken na de operatie).
Structurele gegevens
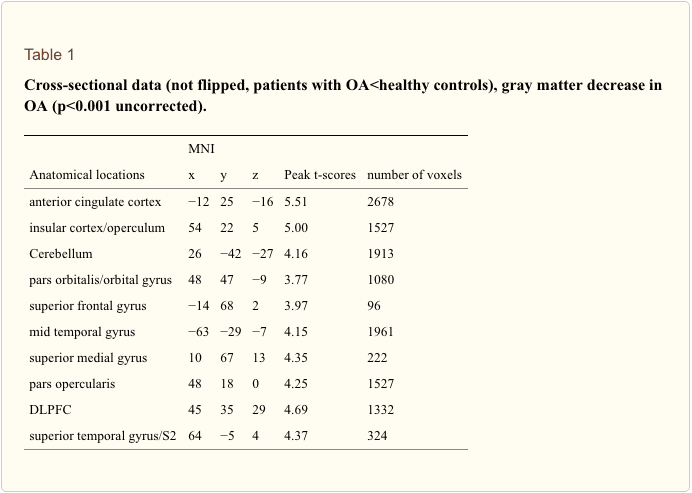
Transversale analyse. We namen leeftijd op als een covariabele in het algemene lineaire model en vonden geen leeftijdsverstoringen. Vergeleken met controles op geslacht en leeftijd, vertoonden patiënten met primaire heupartrose (n?=?20) preoperatief (Scan I) verminderde grijze stof in de cortex anterior cingulate (ACC), de insulaire cortex, operculum, dorsolaterale prefrontale cortex ( DLPFC), rechter temporale pool en cerebellum (tabel 1 en figuur 1). Behalve het rechter putamen (x?=?31, y?=??14, z?=??1; p<0.001, t?=?3.32) werd geen significante toename in grijze stofdichtheid gevonden bij patiënten met artrose vergeleken tot gezonde controles. Door patiënten op tijdpunt scan IV te vergelijken met gematchte controles, werden dezelfde resultaten gevonden als in de cross-sectionele analyse met scan I vergeleken met controles.
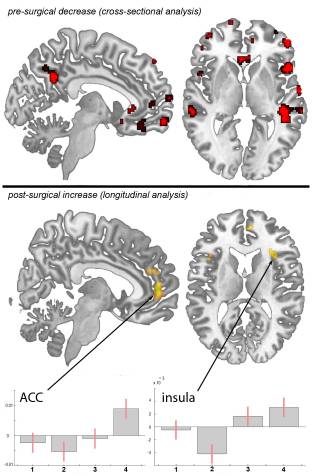
Figuur 1: Statistische parametrische kaarten die de structurele verschillen in grijze stof aantonen bij patiënten met chronische pijn als gevolg van primaire heupartrose in vergelijking met controles en longitudinaal vergeleken met zichzelf in de tijd. Aanzienlijke veranderingen in grijze stof worden in kleur over elkaar heen weergegeven, dwarsdoorsnedegegevens worden in rood weergegeven en longitudinale gegevens in geel. Axiaal vlak: de linkerkant van de afbeelding is de linkerkant van de hersenen. boven: Gebieden met significante afname van grijze stof tussen patiënten met chronische pijn als gevolg van primaire heupartrose en niet-aangetaste controlepersonen. p<0.001 ongecorrigeerde bodem: toename van grijze stof bij 20 pijnvrije patiënten in de derde en vierde scanperiode na een totale heupvervangende operatie, vergeleken met de eerste (preoperatieve) en tweede scan (6 weken na de operatie). p<8 ongecorrigeerde grafieken: contrastschattingen en 0.001% betrouwbaarheidsinterval, effecten van belang, willekeurige eenheden. x-as: contrasten voor de 90 tijdpunten, y-as: contrastschatting op ?4, 3, 50 voor ACC en contrastschatting op 2, 36, 39 voor insula.
Het flippen van de gegevens van patiënten met artrose van de linkerheup (n?=?7) en deze te vergelijken met gezonde controles veranderde de resultaten niet significant, maar voor een afname van de thalamus (x?=?10, y?=??20, z?=?3, p<0.001, t?=?3.44) en een toename van het rechter cerebellum (x?=?25, y?=??37, z?=??50, p<0.001, t? =?5.12) die geen significantie bereikte in de niet-omgedraaide gegevens van de patiënten in vergelijking met controles.
Longitudinale analyse. In de longitudinale analyse werd een significante toename (p<.001 ongecorrigeerd) van grijze stof gedetecteerd door de eerste en tweede scan (chronische pijn/postoperatieve pijn) te vergelijken met de derde en vierde scan (pijnvrij) in de ACC, insulaire cortex, cerebellum en pars orbitalis bij de patiënten met artrose (tabel 2 en figuur 1). Grijze stof nam in de loop van de tijd af (p<.001 analyse van de hele hersenen niet gecorrigeerd) in de secundaire somatosensorische cortex, hippocampus, midcingulate cortex, thalamus en caudate nucleus bij patiënten met artrose (Figuur 2).
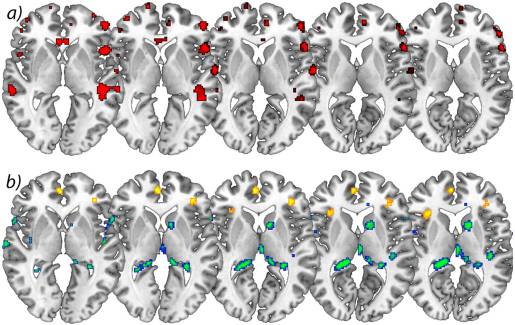
Figuur 2: a) Aanzienlijke toename van grijze hersenstof na succesvolle operatie. Axiale weergave van significante afname van grijze stof bij patiënten met chronische pijn als gevolg van primaire heupartrose in vergelijking met controlepersonen. p<0.001 ongecorrigeerd (transversale analyse), b) Longitudinale toename van grijze stof in de loop van de tijd in geel vergeleken met scan I&IIscan III>scan IV) bij patiënten met artrose. p<0.001 ongecorrigeerd (longitudinale analyse). De linkerkant van de afbeelding is de linkerkant van de hersenen.
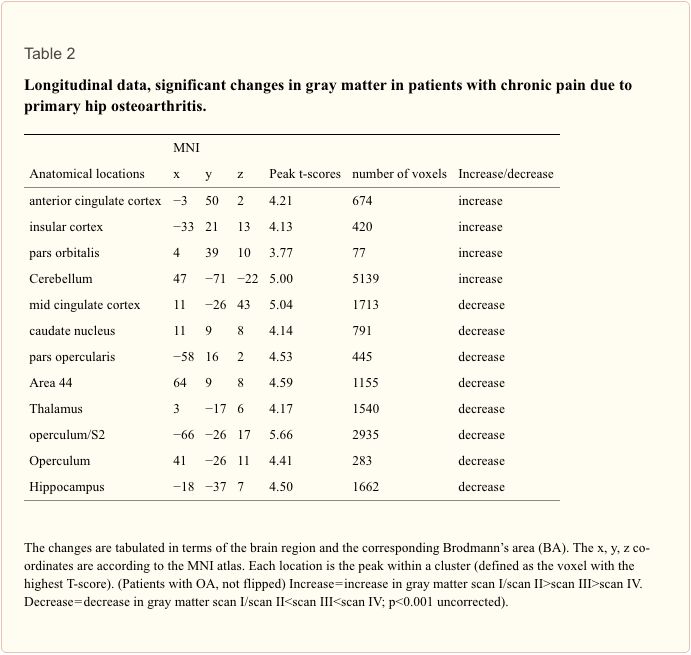
Het spiegelen van de gegevens van patiënten met artrose van de linkerheup (n?=?7) veranderde de resultaten niet significant, maar voor een afname van de grijze hersenstof in de Heschl's Gyrus (x?=??41, y?=?? 21, z?=?10, p<0.001, t?=?3.69) en Precuneus (x?=?15, y?=??36, z?=?3, p<0.001, t?=?4.60) .
Door de eerste scan (preoperatieve) te contrasteren met scans 3+4 (postoperatieve), vonden we een toename van grijze stof in de frontale cortex en motorische cortex (p<0.001 ongecorrigeerd). We merken op dat dit contrast minder streng is omdat we nu minder scans per aandoening hebben (pijn vs. niet-pijn). Wanneer we de drempel verlagen, herhalen we wat we hebben gevonden met contrast van 1+2 vs. 3+4.
Door te zoeken naar gebieden die over alle tijdsintervallen toenemen, vonden we veranderingen in de grijze stof van de hersenen in motorische gebieden (gebied 6) bij patiënten met coxartrose na totale heupprothese (scan Idbm.neuro.uni-jena.de/vbm/) konden we deze bevinding repliceren in de cortex anterior en mid-cingulate en beide anterior insulae.
We berekenden de effectgroottes en de cross-sectionele analyse (patiënten vs. controles) leverde een Cohen�sd van 1.78751 op in de piekvoxel van de ACC (x?=??12, y?=?25, z?=?? 16). We hebben ook Cohen'sd berekend voor de longitudinale analyse (contrastscan 1+2 vs. scan 3+4). Dit resulteerde in een Cohen�sd van 1.1158 in de ACC (x?=??3, y?=?50, z?=?2). Wat betreft de insula (x?=??33, y?=?21, z?=?13) en gerelateerd aan hetzelfde contrast, is Cohen'sd 1.0949. Bovendien hebben we het gemiddelde berekend van de voxelwaarden die niet nul zijn van de Cohen'sd-kaart binnen de ROI (bestaande uit de voorste afdeling van de cingulate gyrus en de subcallosale cortex, afgeleid van de Harvard-Oxford Cortical Structural Atlas): 1.251223.

Insight van Dr. Alex Jimenez
Patiënten met chronische pijn kunnen in de loop van de tijd verschillende gezondheidsproblemen ervaren, naast hun toch al slopende symptomen. Veel mensen zullen bijvoorbeeld slaapproblemen ervaren als gevolg van hun pijn, maar het belangrijkste is dat chronische pijn ook kan leiden tot verschillende psychische problemen, waaronder angst en depressie. De effecten die pijn op de hersenen kan hebben, lijken misschien al te overweldigend, maar groeiend bewijs suggereert dat deze hersenveranderingen niet permanent zijn en kunnen worden teruggedraaid wanneer chronische pijnpatiënten de juiste behandeling krijgen voor hun onderliggende gezondheidsproblemen. Volgens het artikel weerspiegelen afwijkingen van de grijze stof die bij chronische pijn worden gevonden geen hersenbeschadiging, maar zijn ze eerder een omkeerbaar gevolg dat normaliseert wanneer de pijn adequaat wordt behandeld. Gelukkig zijn er verschillende behandelmethoden beschikbaar om chronische pijnsymptomen te verlichten en de structuur en functie van de hersenen te herstellen.
Discussie
Door de hele hersenstructuur in de loop van de tijd te volgen, bevestigen en breiden we onze recentelijk gepubliceerde pilootgegevens uit [17]. We vonden veranderingen in de grijze stof van de hersenen bij patiënten met primaire heupartrose in de chronische pijntoestand, die gedeeltelijk verdwijnen als deze patiënten pijnvrij zijn, na een endoprothetische heupoperatie. De gedeeltelijke toename van grijze stof na de operatie is bijna in dezelfde gebieden waar een afname van grijze stof is waargenomen vóór de operatie. Het omdraaien van de gegevens van patiënten met artrose in de linkerheup (en dus normaliseren voor de pijnzijde) had slechts weinig invloed op de resultaten, maar toonde bovendien een afname van grijze stof in de gyrus van Heschl en Precuneus die we niet gemakkelijk kunnen verklaren en, aangezien er geen a priori hypothese bestaat, moet men deze met grote voorzichtigheid beschouwen. Het verschil dat werd gezien tussen patiënten en gezonde controles bij scan I was echter nog steeds waarneembaar in de cross-sectionele analyse bij scan IV. De relatieve toename van grijze stof in de loop van de tijd is daarom subtiel, dwz niet voldoende duidelijk om een effect te hebben op de transversale analyse, een bevinding die al is aangetoond in onderzoeken naar ervaringsafhankelijke plasticiteit [30], [31]. We merken op dat het feit dat we laten zien dat sommige delen van hersenveranderingen als gevolg van chronische pijn omkeerbaar zijn, niet uitsluit dat sommige andere delen van deze veranderingen onomkeerbaar zijn.
Interessant is dat we hebben waargenomen dat de afname van de grijze stof in de ACC bij chronische pijnpatiënten vóór de operatie 6 weken na de operatie lijkt door te gaan (scan II) en alleen toeneemt naar scan III en IV, mogelijk als gevolg van pijn na de operatie, of afname van motorische functie. Dit is in lijn met de gedragsgegevens van de fysieke mobiliteitsscore opgenomen in de NHP, die postoperatief geen significante verandering vertoonde op tijdstip II, maar significant toenam richting scan III en IV. Merk op dat onze patiënten na de operatie geen pijn in de heup rapporteerden, maar pijn na de operatie ervoeren in de omliggende spieren en huid die door patiënten heel anders werd waargenomen. Omdat patiënten echter nog steeds wat pijn meldden bij scan II, hebben we ook de eerste scan (pre-operatie) vergeleken met scans III + IV (post-operatie), waarbij een toename van grijze stof in de frontale cortex en motorische cortex werd onthuld. We merken op dat dit contrast minder stringent is vanwege minder scans per aandoening (pijn vs. niet-pijn). Toen we de drempel verlaagden, herhalen we wat we hebben gevonden met het contrast van I+II versus III+IV.
Onze gegevens suggereren sterk dat veranderingen in de grijze stof bij chronische pijnpatiënten, die meestal worden aangetroffen in gebieden die betrokken zijn bij supraspinale nociceptieve verwerking [4], niet te wijten zijn aan neuronale atrofie of hersenbeschadiging. Het feit dat deze veranderingen in de toestand van chronische pijn niet volledig omkeren, kan worden verklaard door de relatief korte observatieperiode (een jaar na de operatie versus gemiddeld zeven jaar chronische pijn vóór de operatie). Neuroplastische hersenveranderingen die zich over meerdere jaren kunnen hebben ontwikkeld (als gevolg van constante nociceptieve input) hebben waarschijnlijk meer tijd nodig om volledig om te keren. Een andere mogelijkheid waarom de toename van grijze stof alleen kan worden gedetecteerd in de longitudinale data en niet in de cross-sectionele data (dwz tussen cohorten op tijdstip IV) is dat het aantal patiënten (n?=?20) te klein is. Opgemerkt moet worden dat de variantie tussen hersenen van meerdere individuen vrij groot is en dat longitudinale gegevens het voordeel hebben dat de variantie relatief klein is omdat dezelfde hersenen meerdere keren worden gescand. Bijgevolg zullen subtiele veranderingen alleen in longitudinale gegevens kunnen worden gedetecteerd [30], [31], [32]. Natuurlijk kunnen we niet uitsluiten dat deze veranderingen op zijn minst gedeeltelijk onomkeerbaar zijn, hoewel dat onwaarschijnlijk is, gezien de bevindingen van oefeningsspecifieke structurele plasticiteit en reorganisatie [4], [12], [30], [33], [34]. Om deze vraag te beantwoorden, moeten toekomstige studies patiënten herhaaldelijk over langere tijdsperioden, mogelijk jaren, onderzoeken.
We merken op dat we slechts beperkte conclusies kunnen trekken over de dynamiek van morfologische hersenveranderingen in de loop van de tijd. De reden is dat toen we deze studie in 2007 ontwierpen en in 2008 en 2009 scanden, het niet bekend was of er structurele veranderingen zouden optreden en dat we vanwege de haalbaarheid de scandata en tijdframes hebben gekozen zoals hier beschreven. Men zou kunnen stellen dat de grijze massa in de tijd verandert, die we beschrijven voor de patiëntengroep, ook in de controlegroep zou kunnen zijn opgetreden (tijdseffect). Eventuele veranderingen als gevolg van veroudering, of helemaal niet, zullen echter naar verwachting een afname van het volume zijn. Gezien onze a priori-hypothese, gebaseerd op 9 onafhankelijke onderzoeken en cohorten die een afname van de grijze stof bij chronische pijnpatiënten laten zien [7], [8], [9], [15], [24], [25], [26], [27], [28], hebben we ons gericht op regionale stijgingen in de tijd en daarom geloven we dat onze bevinding geen eenvoudig tijdseffect is. Merk op dat we niet kunnen uitsluiten dat de afname van de grijze stof in de loop van de tijd die we in onze patiëntengroep vonden, te wijten kan zijn aan een tijdseffect, aangezien we onze controlegroep niet in hetzelfde tijdsbestek hebben gescand. Gezien de bevindingen zouden toekomstige studies moeten streven naar meer en kortere tijdsintervallen, aangezien inspanningsafhankelijke morfometrische hersenveranderingen zo snel kunnen optreden als na 1 week [32], [33].
Naast de impact van het nociceptieve aspect van pijn op de grijze stof van de hersenen [17], [34] zagen we dat veranderingen in motorische functie waarschijnlijk ook bijdragen aan de structurele veranderingen. We ontdekten dat motorische en premotorische gebieden (gebied 6) over alle tijdsintervallen toenamen (Figuur 3). Intuïtief kan dit te wijten zijn aan een verbetering van de motorische functie in de loop van de tijd, aangezien de patiënten niet meer beperkt waren in het leiden van een normaal leven. Met name hebben we ons niet gericht op motorische functie, maar op een verbetering van pijnervaring, gezien onze oorspronkelijke zoektocht om te onderzoeken of de bekende vermindering van hersengrijze stof bij chronische pijnpatiënten in principe omkeerbaar is. Daarom hebben we geen specifieke instrumenten gebruikt om de motorische functie te onderzoeken. Niettemin is (functionele) reorganisatie van de motorische cortex bij patiënten met pijnsyndromen goed gedocumenteerd [35], [36], [37], [38]. Bovendien is de motorische cortex een doelwit in therapeutische benaderingen bij medisch onhandelbare chronische pijnpatiënten met behulp van directe hersenstimulatie [39], [40], transcraniële gelijkstroomstimulatie [41] en repetitieve transcraniële magnetische stimulatie [42], [43]. De exacte mechanismen van een dergelijke modulatie (facilitatie versus remming, of eenvoudigweg interferentie in de pijngerelateerde netwerken) zijn nog niet opgehelderd [40]. Een recente studie toonde aan dat een specifieke motorische ervaring de structuur van de hersenen kan veranderen [13]. Synaptogenese, reorganisatie van bewegingsrepresentaties en angiogenese in de motorische cortex kunnen optreden met speciale eisen van een motorische taak. Tsao et al. toonde reorganisatie in de motorische cortex van patiënten met chronische lage-rugpijn die specifiek voor rugpijn lijken te zijn [44] en Puri et al. waargenomen een vermindering van de linker aanvullende motorische grijze stof bij patiënten met fibromyalgie [45]. Onze studie was niet ontworpen om de verschillende factoren te ontwarren die de hersenen bij chronische pijn kunnen veranderen, maar we interpreteren onze gegevens over de veranderingen in de grijze stof dat ze niet uitsluitend de gevolgen van constante nociceptieve input weerspiegelen. In feite wees een recent onderzoek bij neuropathische pijnpatiënten op afwijkingen in hersengebieden die emotionele, autonome en pijnperceptie omvatten, wat impliceert dat ze een cruciale rol spelen in het globale klinische beeld van chronische pijn [28].
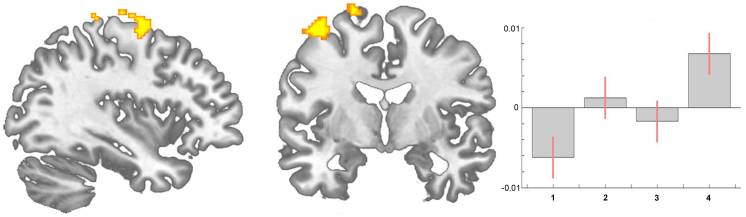
Figuur 3: Statistische parametrische kaarten die een significante toename van grijze hersenstof in motorische gebieden (gebied 6) aantonen bij patiënten met coxartrose vóór in vergelijking met na THR (longitudinale analyse, scan I Contrastschattingen bij x?=?19, y?=??12, z?=?70.
Twee recente pilotstudies waren gericht op heupvervangingstherapie bij artrosepatiënten, het enige chronische pijnsyndroom dat in principe te genezen is met totale heupvervanging [17], [46] en deze gegevens worden geflankeerd door een zeer recente studie bij patiënten met chronische lage-rugpijn [ 47]. Deze onderzoeken moeten worden gezien in het licht van verschillende longitudinale onderzoeken naar ervaringsafhankelijke neuronale plasticiteit bij mensen op structureel niveau [30], [31] en een recent onderzoek naar structurele hersenveranderingen bij gezonde vrijwilligers die herhaalde pijnlijke stimulatie ervaren [34] . De kernboodschap van al deze onderzoeken is dat het belangrijkste verschil in de hersenstructuur tussen pijnpatiënten en controles kan verdwijnen wanneer de pijn is genezen. Er moet echter rekening mee worden gehouden dat het eenvoudigweg niet duidelijk is of de veranderingen bij chronische pijnpatiënten alleen te wijten zijn aan nociceptieve input of aan de gevolgen van pijn of beide. Het is meer dan waarschijnlijk dat gedragsveranderingen, zoals ontbering of verbetering van sociale contacten, behendigheid, fysieke training en veranderingen in levensstijl voldoende zijn om de hersenen vorm te geven [6], [12], [28], [48]. Vooral depressie als comorbiditeit of gevolg van pijn is een belangrijke kandidaat om de verschillen tussen patiënten en controles te verklaren. Een kleine groep van onze patiënten met artrose vertoonde milde tot matige depressieve symptomen die met de tijd veranderden. We vonden de structurele veranderingen niet significant covariëren met de BDI-score, maar de vraag rijst hoeveel andere gedragsveranderingen door het ontbreken van pijn en motorische verbetering kunnen bijdragen aan de resultaten en in welke mate ze dat doen. Deze gedragsveranderingen kunnen mogelijk een afname van de grijze stof bij chronische pijn beïnvloeden, evenals een toename van de grijze stof als de pijn weg is.
Een andere belangrijke factor die onze interpretatie van de resultaten kan vertekenen, is het feit dat bijna alle patiënten met chronische pijn pijnstillers slikten, die ze stopten toen ze pijnvrij waren. Men zou kunnen stellen dat NSAID's zoals diclofenac of ibuprofen enige effecten hebben op neurale systemen en hetzelfde geldt voor opioïden, anti-epileptica en antidepressiva, medicijnen die vaak worden gebruikt bij chronische pijntherapie. De impact van pijnstillers en andere medicijnen op morfometrische bevindingen kan belangrijk zijn (48). Geen enkele studie heeft tot nu toe effecten van pijnmedicatie op de hersenmorfologie aangetoond, maar verschillende artikelen hebben aangetoond dat veranderingen in de hersenstructuur bij chronische pijnpatiënten niet alleen worden verklaard door pijngerelateerde inactiviteit [15], noch door pijnmedicatie [7], [9], [49]. Specifieke studies ontbreken echter. Verder onderzoek zou zich moeten richten op de ervaringsafhankelijke veranderingen in corticale plasticiteit, die enorme klinische implicaties kunnen hebben voor de behandeling van chronische pijn.
We vonden ook afnames van grijze stof in de longitudinale analyse, mogelijk als gevolg van reorganisatieprocessen die gepaard gaan met veranderingen in motorische functie en pijnperceptie. Er is weinig informatie beschikbaar over longitudinale veranderingen in de grijze stof van de hersenen bij pijnaandoeningen, daarom hebben we geen hypothese voor een afname van de grijze stof in deze gebieden na de operatie. Teutsch et al. [25] vond een toename van grijze hersenstof in de somatosensorische en midcingulate cortex bij gezonde vrijwilligers die gedurende acht opeenvolgende dagen pijnlijke stimulatie ervoeren in een dagelijks protocol. De bevinding van een toename van grijze stof na experimentele nociceptieve input overlapt anatomisch tot op zekere hoogte met de afname van grijze stof in de hersenen in deze studie bij patiënten die genezen waren van langdurige chronische pijn. Dit impliceert dat nociceptieve input bij gezonde vrijwilligers leidt tot inspanningsafhankelijke structurele veranderingen, zoals mogelijk het geval is bij patiënten met chronische pijn, en dat deze veranderingen bij gezonde vrijwilligers omkeren wanneer nociceptieve input stopt. Bijgevolg kan de afname van grijze stof in deze gebieden die bij patiënten met artrose wordt gezien, worden geïnterpreteerd als hetzelfde fundamentele proces: inspanningsafhankelijke veranderingen in de hersenen veranderen [50]. Als een niet-invasieve procedure is MR-morfometrie het ideale hulpmiddel voor het zoeken naar de morfologische substraten van ziekten, het verdiepen van ons begrip van de relatie tussen hersenstructuur en -functie, en zelfs om therapeutische interventies te volgen. Een van de grote uitdagingen in de toekomst is om dit krachtige hulpmiddel aan te passen voor multicentrische en therapeutische onderzoeken naar chronische pijn.
Beperkingen van deze studie
Hoewel deze studie een uitbreiding is van onze eerdere studie, waarbij de follow-upgegevens werden uitgebreid tot 12 maanden en meer patiënten werden onderzocht, is onze principiële bevinding dat morfometrische hersenveranderingen bij chronische pijn omkeerbaar zijn nogal subtiel. De effectgroottes zijn klein (zie hierboven) en de effecten worden deels gedreven door een verdere vermindering van het regionale hersengrijze stofvolume op het tijdstip van scan 2. Wanneer we de gegevens uit scan 2 (direct na de operatie) uitsluiten, is alleen significant toenames in grijze hersenstof voor motorische cortex en frontale cortex overleven een drempel van p<0.001 ongecorrigeerd (tabel 3).
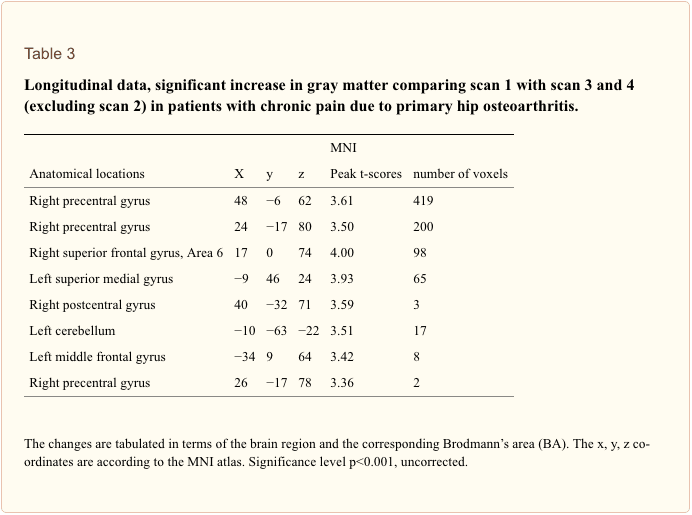
Conclusie
Het is niet mogelijk om te onderscheiden in hoeverre de structurele veranderingen die we hebben waargenomen het gevolg zijn van veranderingen in nociceptieve input, veranderingen in motorische functie of medicatiegebruik of veranderingen in het welzijn als zodanig. Door de groepscontrasten van de eerste en laatste scan met elkaar te maskeren kwamen veel minder verschillen naar voren dan verwacht. Vermoedelijk ontwikkelen hersenveranderingen als gevolg van chronische pijn, met alle gevolgen van dien, zich over een vrij lange tijdsperiode en kunnen ook enige tijd nodig hebben om terug te keren. Niettemin onthullen deze resultaten reorganisatieprocessen, wat sterk suggereert dat chronische nociceptieve input en motorische stoornissen bij deze patiënten leiden tot veranderde verwerking in corticale regio's en bijgevolg structurele hersenveranderingen die in principe omkeerbaar zijn.
Dankwoord
We danken alle vrijwilligers voor de deelname aan deze studie en de Physics and Methods-groep bij NeuroImage Nord in Hamburg. De studie kreeg ethische goedkeuring van de lokale ethische commissie en voorafgaand aan het onderzoek werd schriftelijke geïnformeerde toestemming verkregen van alle deelnemers aan de studie.
Financieringsverklaring
Dit werk werd ondersteund door subsidies van de DFG (Duitse onderzoeksstichting) (MA 1862/2-3) en BMBF (het federale ministerie van onderwijs en onderzoek) (371 57 01 en NeuroImage Nord). De financiers hadden geen rol bij het ontwerp van de studie, het verzamelen en analyseren van gegevens, de beslissing om het manuscript te publiceren of de voorbereiding van het manuscript.
Het endocannabinoïdesysteem: het essentiële systeem waar je nog nooit van hebt gehoord
Als je nog nooit van het endocannabinoïdesysteem of ECS hebt gehoord, hoef je je niet te schamen. In de jaren zestig isoleerden de onderzoekers die geïnteresseerd raakten in de biologische activiteit van cannabis, uiteindelijk veel van de actieve chemicaliën. Het duurde echter nog 1960 jaar voordat onderzoekers die diermodellen bestudeerden een receptor voor deze ECS-chemicaliën in de hersenen van knaagdieren vonden, een ontdekking die een hele wereld van onderzoek opende naar het bestaan van ECS-receptoren en wat hun fysiologische doel is.
We weten nu dat de meeste dieren, van vissen tot vogels tot zoogdieren, een endocannabinoïde bezitten, en we weten dat mensen niet alleen hun eigen cannabinoïden maken die interageren met dit specifieke systeem, maar we produceren ook andere verbindingen die interageren met het ECS, die van die worden waargenomen in veel verschillende planten en voedingsmiddelen, veel verder dan de cannabissoorten.
Als systeem van het menselijk lichaam is het ECS geen geïsoleerd structureel platform zoals het zenuwstelsel of het cardiovasculaire systeem. In plaats daarvan is de ECS een reeks receptoren die wijdverbreid door het lichaam zijn verspreid en die worden geactiveerd door een reeks liganden die we gezamenlijk kennen als endocannabinoïden of endogene cannabinoïden. Beide geverifieerde receptoren worden gewoon CB1 en CB2 genoemd, hoewel er andere zijn voorgesteld. PPAR- en TRP-kanalen bemiddelen ook voor sommige functies. Evenzo vindt u slechts twee goed gedocumenteerde endocannabinoïden: anadamide en 2-arachidonoylglycerol, of 2-AG.
Bovendien zijn de enzymen die de endocannabinoïden synthetiseren en afbreken van fundamenteel belang voor het endocannabinoïdesysteem. Endocannabinoïden worden verondersteld te worden gesynthetiseerd in een basis die nodig is. De belangrijkste betrokken enzymen zijn diacylglycerol lipase en N-acyl-fosfatidylethanolamine-fosfolipase D, die respectievelijk 2-AG en anandamide synthetiseren. De twee belangrijkste afbrekende enzymen zijn vetzuuramidehydrolase, of FAAH, dat anandamide afbreekt, en monoacylglycerollipase, of MAGL, dat 2-AG afbreekt. De regulatie van deze twee enzymen kan de modulatie van de ECS verhogen of verlagen.
Wat is de functie van het ECS?
De ECS is het belangrijkste homeostatische regelsysteem van het lichaam. Het kan gemakkelijk worden gezien als het interne adaptogene systeem van het lichaam, dat altijd werkt om het evenwicht tussen verschillende functies te behouden. Endocannabinoïden werken in grote lijnen als neuromodulatoren en reguleren als zodanig een breed scala aan lichamelijke processen, van vruchtbaarheid tot pijn. Enkele van die bekendere functies van de ECS zijn als volgt:
Zenuwgestel
Vanuit het centrale zenuwstelsel, of het CZS, zal algemene stimulatie van de CB1-receptoren de afgifte van glutamaat en GABA remmen. In het CZS speelt het ECS een rol bij geheugenvorming en leren, bevordert het neurogenese in de hippocampus en reguleert het ook de neuronale prikkelbaarheid. Het ECS speelt ook een rol in de manier waarop de hersenen zullen reageren op letsel en ontsteking. Vanuit het ruggenmerg moduleert het ECS de pijnsignalering en stimuleert het de natuurlijke pijnstilling. In het perifere zenuwstelsel, waarin de CB2-receptoren de controle uitoefenen, werkt het ECS voornamelijk in het sympathische zenuwstelsel om de functies van de darmen, de urinewegen en de voortplantingsorganen te reguleren.
Stress en stemming
De ECS heeft meerdere effecten op stressreacties en emotionele regulatie, zoals het initiëren van deze lichamelijke reactie op acute stress en aanpassing in de loop van de tijd aan meer langdurige emoties, zoals angst en angst. Een gezond werkend endocannabinoïdesysteem is van cruciaal belang voor hoe mensen moduleren tussen een bevredigende mate van opwinding in vergelijking met een niveau dat buitensporig en onaangenaam is. Het ECS speelt ook een rol bij geheugenvorming en mogelijk vooral bij de manier waarop de hersenen herinneringen van stress of letsel inprenten. Omdat het ECS de afgifte van dopamine, noradrenaline, serotonine en cortisol moduleert, kan het ook de emotionele respons en het gedrag op grote schaal beïnvloeden.
spijsverteringsorganen
Het spijsverteringskanaal is bevolkt met zowel CB1- als CB2-receptoren die verschillende belangrijke aspecten van de GI-gezondheid reguleren. Er wordt gedacht dat de ECS de "missing link" zou kunnen zijn bij het beschrijven van de darm-hersen-immuun link die een belangrijke rol speelt in de functionele gezondheid van het spijsverteringskanaal. Het ECS is een regulator van de darmimmuniteit, misschien door het immuunsysteem te beperken om gezonde flora te vernietigen, en ook door de modulatie van cytokinesignalering. De ECS moduleert de natuurlijke ontstekingsreactie in het spijsverteringskanaal, wat belangrijke implicaties heeft voor een breed scala aan gezondheidsproblemen. Maag- en algemene GI-motiliteit lijkt ook gedeeltelijk te worden bepaald door de ECS.
Eetlust en metabolisme
De ECS, met name de CB1-receptoren, spelen een rol bij de eetlust, het metabolisme en de regulatie van lichaamsvet. Stimulatie van de CB1-receptoren verhoogt het voedselzoekgedrag, verbetert het geurbewustzijn en reguleert ook de energiebalans. Zowel dieren als mensen met overgewicht hebben ECS-ontregeling waardoor dit systeem hyperactief kan worden, wat bijdraagt aan zowel te veel eten als verminderd energieverbruik. Er is aangetoond dat de circulerende niveaus van anandamide en 2-AG verhoogd zijn bij obesitas, wat gedeeltelijk te wijten kan zijn aan een verminderde productie van het FAAH-afbrekende enzym.
Immuungezondheid en ontstekingsreactie
De cellen en organen van het immuunsysteem zijn rijk aan endocannabinoïde-receptoren. Cannabinoïde-receptoren komen tot expressie in de thymusklier, milt, amandelen en beenmerg, evenals op T- en B-lymfocyten, macrofagen, mestcellen, neutrofielen en natuurlijke killercellen. De ECS wordt beschouwd als de belangrijkste aanjager van de balans en homeostase van het immuunsysteem. Hoewel niet alle functies van het ECS van het immuunsysteem worden begrepen, lijkt het ECS de productie van cytokines te reguleren en ook een rol te spelen bij het voorkomen van overactiviteit in het immuunsysteem. Ontsteking is een natuurlijk onderdeel van de immuunrespons en speelt een heel normale rol bij acute beledigingen van het lichaam, waaronder verwondingen en ziekten; niettemin, als het niet onder controle wordt gehouden, kan het chronisch worden en bijdragen aan een cascade van nadelige gezondheidsproblemen, zoals chronische pijn. Door de immuunrespons onder controle te houden, helpt de ECS om een meer evenwichtige ontstekingsreactie door het lichaam te behouden.
Andere door de ECS gereguleerde gezondheidsgebieden:
- Gezondheid van de botten
- Vruchtbaarheid
- Gezondheid van de huid
- Arteriële en respiratoire gezondheid
- Slaap en circadiaans ritme
Hoe u een gezond ECS het beste kunt ondersteunen, is een vraag die veel onderzoekers nu proberen te beantwoorden. Blijf ons volgen voor meer informatie over dit opkomende onderwerp.
Concluderend�chronische pijn is in verband gebracht met veranderingen in de hersenen, waaronder de vermindering van grijze stof. Het bovenstaande artikel toonde echter aan dat chronische pijn de algehele structuur en functie van de hersenen kan veranderen. Hoewel chronische pijn hiertoe kan leiden, naast andere gezondheidsproblemen, kan de juiste behandeling van de onderliggende symptomen van de patiënt hersenveranderingen omkeren en grijze stof reguleren. Bovendien zijn er steeds meer onderzoeken naar voren gekomen over het belang van het endocannabinoïdesysteem en zijn functie bij het beheersen en beheersen van chronische pijn en andere gezondheidsproblemen. Informatie waarnaar wordt verwezen door het National Center for Biotechnology Information (NCBI). De reikwijdte van onze informatie is beperkt tot zowel chiropractie als letsels en aandoeningen van de wervelkolom. Als u het onderwerp wilt bespreken, kunt u het aan Dr. Jimenez vragen of contact met ons opnemen via�915-850-0900 .
Curator van Dr. Alex Jimenez
Bijkomende onderwerpen: Rugpijn
Rugpijn is een van de meest voorkomende oorzaken van invaliditeit en gemiste dagen op het werk wereldwijd. Rugpijn is trouwens toegeschreven als de op één na meest voorkomende reden voor bezoeken aan artsenbureaus, die in de minderheid zijn dan alleen infecties aan de bovenste luchtwegen. Ongeveer 80 procent van de bevolking ervaart ten minste één keer gedurende hun hele leven een vorm van rugpijn. De wervelkolom is een complexe structuur bestaande uit botten, gewrichten, ligamenten en spieren, naast andere zachte weefsels. Vanwege dit, verwondingen en / of verergerde omstandigheden, zoals herniated discs, kan uiteindelijk leiden tot symptomen van rugpijn. Sportblessures of ongevallen met auto-ongelukken zijn vaak de meest voorkomende oorzaak van rugpijn, maar soms kunnen de eenvoudigste bewegingen pijnlijke resultaten hebben. Gelukkig kunnen alternatieve behandelingsopties, zoals chiropractische zorg, de rugpijn verlichten door het gebruik van spinale aanpassingen en handmatige manipulaties, waardoor uiteindelijk de pijnverlichting wordt verbeterd.

EXTRA BELANGRIJK ONDERWERP: Beheer van lage rugpijn
MEER ONDERWERPEN: EXTRA EXTRA: Chronische pijn en behandelingen
Blanco
Referenties
Accordeon sluiten
Professionele reikwijdte van de praktijk *
De informatie hierin over "Hersenenveranderingen geassocieerd met chronische pijn" is niet bedoeld ter vervanging van een een-op-een relatie met een gekwalificeerde zorgverlener of gediplomeerde arts en is geen medisch advies. We moedigen u aan om beslissingen over de gezondheidszorg te nemen op basis van uw onderzoek en samenwerking met een gekwalificeerde zorgverlener.
Blog Informatie & Scope Discussies
Ons informatiebereik: is beperkt tot chiropractie, musculoskeletale, fysieke medicijnen, welzijn, bijdragende etiologische viscerosomatische stoornissen binnen klinische presentaties, geassocieerde somatoviscerale reflex klinische dynamiek, subluxatiecomplexen, gevoelige gezondheidskwesties en/of functionele geneeskunde artikelen, onderwerpen en discussies.
Wij bieden en presenteren klinische samenwerking met specialisten uit verschillende disciplines. Elke specialist wordt beheerst door hun professionele praktijk en hun jurisdictie van licentiestatus. We gebruiken functionele gezondheids- en welzijnsprotocollen om de verwondingen of aandoeningen van het bewegingsapparaat te behandelen en te ondersteunen.
Onze video's, berichten, onderwerpen, onderwerpen en inzichten behandelen klinische zaken, problemen en onderwerpen die verband houden met en direct of indirect onze klinische praktijk ondersteunen.*
Ons kantoor heeft redelijkerwijs geprobeerd om ondersteunende citaten te geven en heeft de relevante onderzoeksstudie of studies geïdentificeerd die onze berichten ondersteunen. Wij verstrekken kopieën van ondersteunende onderzoeksstudies die op verzoek beschikbaar zijn voor regelgevende instanties en het publiek.
We begrijpen dat we zaken behandelen die een aanvullende uitleg vereisen over hoe het kan helpen bij een bepaald zorgplan of behandelprotocol; daarom, om het onderwerp hierboven verder te bespreken, aarzel dan niet om te vragen Dr. Alex Jimenez, DC, of neem contact met ons op 915-850-0900.
Wij zijn er om u en uw gezin te helpen.
zegeningen
Dr. Alex Jimenez DC MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
e-mail: coach@elpasofunctionalmedicine.com
Licentie als Doctor of Chiropractic (DC) in Texas & New Mexico*
Texas DC-licentie # TX5807, New Mexico DC-licentie # NM-DC2182
Licentie als geregistreerde verpleegkundige (RN*) in Florida
Florida-licentie RN-licentie # RN9617241 (controle nr. 3558029)
Compacte status: Licentie voor meerdere staten: Geautoriseerd om te oefenen in 40 Staten*
Dr. Alex Jimenez DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Mijn digitale visitekaartje