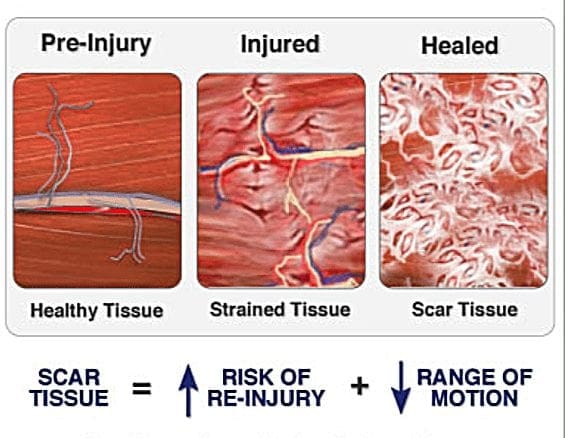
Pijnmodulatiewegmechanismen in El Paso, TX
De meeste, zo niet alle, kwalen van het lichaam veroorzaken pijn. Pijn wordt geïnterpreteerd en waargenomen in de hersenen. Pijn wordt gemoduleerd door twee belangrijke soorten medicijnen die op de hersenen werken: analgetica en anesthetica. De term analgeticum verwijst naar een medicijn dat pijn verlicht zonder bewustzijnsverlies. De uitdrukking centrale anesthesie verwijst naar een medicijn dat het CZS onderdrukt. Het onderscheidt zich door het ontbreken van alle waarneming van zintuiglijke modaliteiten, bijvoorbeeld bewustzijnsverlies zonder verlies van kritieke functies.
Opiaat analgesie (OA)
De meest succesvolle klinisch gebruikte medicijnen voor het produceren van tijdelijke analgesie en verlichting van pijn zijn de opioïdenfamilie, die morfine en heroïne omvat. Er zijn momenteel geen aanvullende krachtige pijntherapeutische opties voor opiaten. Verschillende bijwerkingen veroorzaakt door opiaatgebruik zijn tolerantie en drugsverslaving of verslaving. Over het algemeen moduleren deze medicijnen de binnenkomende pijninformatie in de wervelkolom en het centrale zenuwstelsel, naast het tijdelijk verlichten van pijn, en kunnen ze ook opiaatproducerende analgesie (OA) worden genoemd. Opiaatantagonist is een medicijn dat de opioïde effecten tegenwerkt, zoals naloxon of maltroxon, enz. Het zijn competitieve antagonisten van opiaatreceptoren. De hersenen hebben echter een neuronaal circuit en endogene stoffen die pijn moduleren.
Endogene opioïden
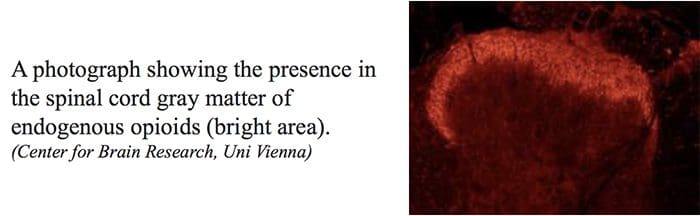
Opioïde neurotransmissie is overal in de hersenen en het ruggenmerg gelokaliseerd en wordt verondersteld veel functies van het centrale zenuwstelsel of het CZS te beïnvloeden, zoals nociceptie, cardiovasculaire functies, thermoregulatie, ademhaling, neuro-endocriene functies, neuro-immuunfuncties, voedselconsumptie, seksuele activiteit, competitieve motorisch gedrag, evenals geheugen en leren. Opioïden hebben een duidelijk effect op de stemming en motivatie en veroorzaken een gevoel van euforie.
Er worden drie klassen van opioïde receptoren geïdentificeerd: -mu, ?-delta en ?-kappa. Alle 3 klassen zijn wijd verspreid in de hersenen. De genen die voor elk van deze coderen, zijn gekloond en bleken te functioneren als leden van de G-eiwitreceptoren. Bovendien zijn in het centrale zenuwstelsel drie hoofdtypen endogene opioïde peptiden die een interactie aangaan met de bovengenoemde opiaatreceptoren herkend, waaronder ?-endorfines, enkefalines en de dynorfines. Deze 3 opioïde peptiden zijn afgeleid van een grote eiwitreceptor door drie verschillende genen, zoals het proopiomelanocortine- of POMC-gen, het proenkefaline-gen en het prodynorfine-gen. De opioïde peptiden moduleren de nociceptieve input op twee manieren: ten eerste blokkeren ze de neurotransmitter vrijkomen door de instroom van Ca2+ in het presynaptische uiteinde te remmen, of ten tweede openen ze kaliumkanalen, die neuronen hyperpolariseren en piekactiviteit remmen. Ze werken op verschillende receptoren in de hersenen en het ruggenmerg.
Enkefalines worden beschouwd als de vermeende liganden voor de ? receptoren, ? endorfines voor de ?-receptoren en dynorfines voor de ? receptoren. De verschillende soorten opioïde receptoren zijn verschillend verdeeld binnen het perifere en centrale zenuwstelsel, of CZS. Er is bewijs voor functionele verschillen in deze receptoren in verschillende structuren. Dit verklaart waarom veel ongewenste bijwerkingen optreden na opiaatbehandelingen. Zo zijn mu(?)-receptoren wijdverbreid in de parabrachiale kernen van de hersenstam, waar een ademhalingscentrum en remming van deze neuronen een zogenaamde ademhalingsdepressie kunnen veroorzaken.
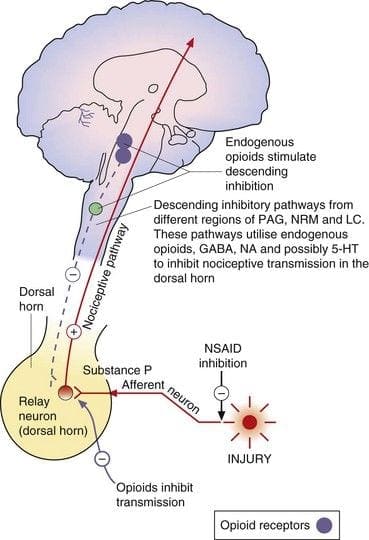
Centrale of perifere uiteinden van nociceptieve afferente vezels bevatten opiaatreceptoren waarin exogene en endogene opioïden zouden kunnen werken om het vermogen om nociceptieve informatie door te geven te moduleren. Bovendien worden hoge dichtheden van opiaatreceptoren gevonden in periaqueductaal grijs, of PAG, nucleus raphe magnus, of NRM, en dorsale raphe, of DR, van de rostrale ventrale medulla, in het ruggenmerg, caudate nucleus, of CN, septum nucleus, hypothalamus, habenula en hippocampus. Systemisch toegediende opioïden in analgetische doseringen activeren spinale en supraspinale mechanismen via ?, ?, en ? type opioïde receptoren en reguleren pijnsignalen om symptomen te moduleren.
Neuronale circuits en pijnmodulatie
Vele decennia lang werd gesuggereerd dat er ergens in het centrale zenuwstelsel een circuit is dat binnenkomende pijndetails kan moduleren. De gate-control-theorie en het stijgende/dalende pijntransmissiesysteem zijn twee suggesties van zo'n circuit. Hieronder zullen we beide in meer detail bespreken.
Gate Control Theorie
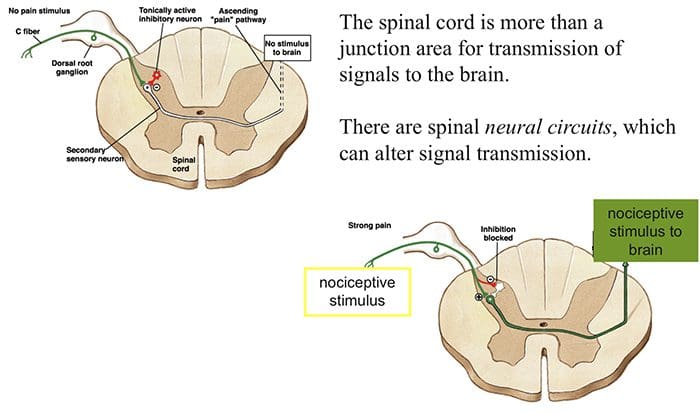
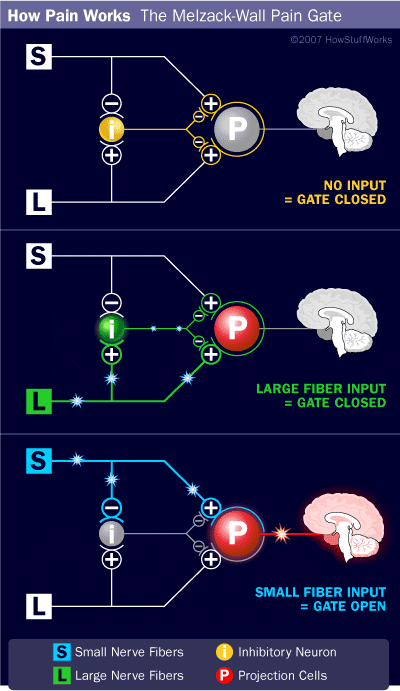
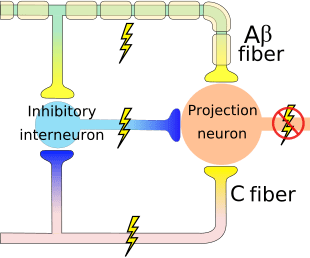
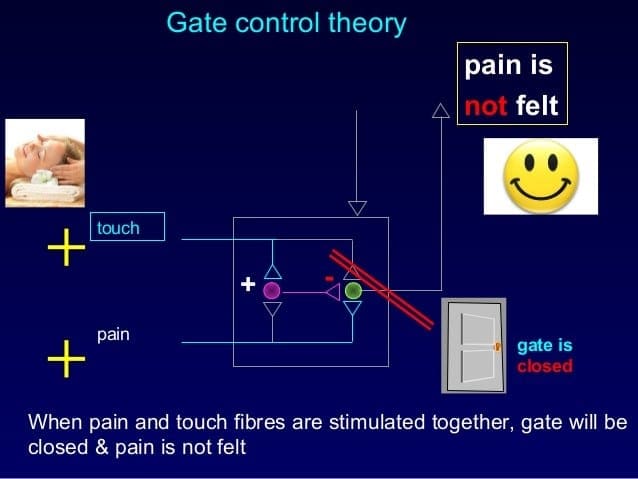
Het aanvankelijke pijnmodulerende mechanisme dat bekend staat als de gate control theorie, is halverwege de jaren zestig door Melzack en Wall voorgesteld. Het idee van de poortcontroletheorie is dat niet-pijnlijke input de poorten sluit voor pijnlijke input, wat resulteert in het vermijden van de pijnsensatie van reizen naar het CZS, bijvoorbeeld niet-schadelijke input of stimulatie, onderdrukt pijn.
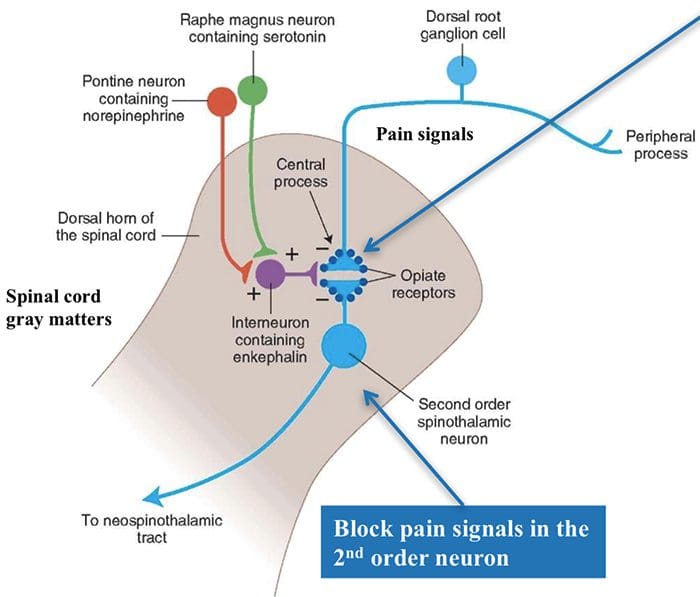
De theorie houdt in dat collateralen van de grote sensorische vezels die cutane sensorische input dragen, remmende interneuronen activeren, die de pijnoverdrachtsgegevens die door de pijnvezels worden overgedragen, remmen en reguleren. Niet-schadelijke input remt pijn, of sensorische input, en sluit de poort naar schadelijke input. De poortcontroletheorie toont aan dat op het niveau van het ruggenmerg, niet-schadelijke stimulatie presynaptische remming zal veroorzaken op de nociceptorvezels van de dorsale wortel die synapsen op nociceptoren spinale neuronen (T). Deze presynaptische remming zal ook voorkomen dat binnenkomende schadelijke informatie het CZS bereikt, het zal bijvoorbeeld de poort sluiten voor binnenkomende giftige informatie.
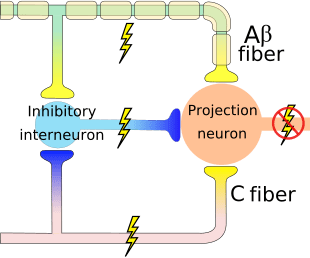
De gate-control-theorie was de grondgedachte voor het idee achter de productie en het gebruik van de transcutane elektrische zenuwstimulatie, of TENS, voor pijnverlichting. Om effectief te zijn, genereert de TENS-eenheid twee verschillende huidige frequenties onder de pijngrens die de patiënt kan nemen. Dit proces heeft een zekere mate van succes gevonden in de behandeling van chronische pijn.
Pijnmodulatie: Gate Control Theorie
Stimulatie geproduceerde analgesie (SPA)
Bewijs voor een inherent analgesiesysteem werd gevonden door intracraniële elektrische stimulatie van bepaalde discrete hersengebieden. Deze gebieden zijn het periaqueductale grijs, of PAG, en nucleus raphe magnus, of NRM, dorsale raphe, of DR, caudate nucleus, of CN, septum nucleus, of Spt, samen met andere kernen. Dergelijke stimulatie of zintuiglijke signalen, remt pijn, maakt analgesie zonder gedragsonderdrukking, terwijl de tast-, temperatuur- en druksensatie intact blijft. Volgens onderzoeksstudies is SPA, of stimulatie-geproduceerde analgesie, meer uitgesproken en duurt het langer na stimulatie bij mensen dan bij proefdieren. Bovendien reageren de proefpersonen tijdens SPA echter nog steeds op niet-pijnlijke stimulatie zoals temperatuur en aanraking binnen het omschreven gebied van analgesie. De meest effectieve CNS, of regio's van het centrale zenuwstelsel voor het optreden van SPA, zijn in de PAG en de raphe-kernen, of RN.
Elektrische stimulatie van PAG of NRM remt spinale thalamische cellen, of spinale neuronen die monosynaptisch naar de thalamus projecteren, in laminae I, II en V om de schadelijke informatie van de nociceptoren te verzekeren die uiteindelijk worden gemoduleerd in het niveau van het ruggenmerg. Bovendien heeft PAG neuronale verbindingen met de nucleus raphe magnus of NRM.
De activiteit van de PAG vindt hoogstwaarschijnlijk plaats door activering van de dalende route van NRM en waarschijnlijk ook door activering van stijgende verbindingen die werken op grotere subcorticale niveaus van het CZS. Bovendien produceert elektrische stimulatie van PAG of NRM gedragsanalgesie of veroorzaakte stimulatie analgesie. Stimulatie veroorzaakte analgesie, of SPA, veroorzaakt de afgifte van endorfines die kunnen worden geblokkeerd door de opiaatantagonist naloxon.
Tijdens PAG- en/of RN-stimulatie kan serotonine, ook medisch aangeduid als 5-HT, ook worden afgevoerd uit stijgende en dalende axonen van subcorticale kernen, in spinale trigeminuskernen en in het ruggenmerg. Deze afgifte van 5-HT moduleert en reguleert pijnoverdracht door inkomende neurale actie te remmen of te blokkeren. Uitputting van 5-HT door elektrische laesie van de raphe-kernen of met een neurotoxische laesie veroorzaakt door lokale injectie van een chemisch agens zoals parachloorfenylalanine of PCPA, resulteert in het blokkeren van de kracht van opiaat, zowel intracraniaal als systemisch, evenals die van elektrische stimulatie om analgesie te produceren.
Om te bevestigen of de elektrische stimulatie analgesie veroorzaakte via de afgifte van opiaat en dopamine, wordt de regio lokaal micro-geïnjecteerd met morfine of 5-HT. Al deze micro-injecties zorgen uiteindelijk voor analgesie. Deze processen bieden ook een manier om hersengebieden te identificeren die verband houden met pijnonderdrukking en helpen bij het maken van een kaart van pijncentra. De meest effectieve manier om opiaat-analgesie of OA te produceren, is door intracerebrale injectie van morfine in de PAG.
De PAG en RN, evenals andere hersenstructuren waarin analgesie wordt geproduceerd, zijn ook rijk aan opiaatreceptoren. Intracerebrale toediening van opioïden veroorzaakte analgesie en SPA kan worden geblokkeerd door systemische of door lokale micro-injecties van naloxon, de morfine-antagonist, in de PAG of RN. Om die reden is er gesuggereerd dat de twee, zowel OA als SPA, volgens een frequent mechanisme werken.
Als OA en SPA zich via hetzelfde intrinsieke systeem gedragen, is de hypothese dat opiaten een pijnonderdrukkingsmechanisme activeren veel waarschijnlijker. In feite suggereert het huidige bewijs dat micro-injecties van een opiaat in de PAG een efferente hersenstamsysteem activeren dat de overdracht van pijn op segmentale niveaus van het ruggenmerg remt. Deze waarnemingen impliceren dat analgesie die wordt opgewekt door het periaqueductale grijs, of PAG, een dalende weg naar het ruggenmerg vereist.

Insight van Dr. Alex Jimenez
Pijnmodulatie vindt plaats door het proces van elektrische hersenstimulatie die optreedt als gevolg van de activering van dalende remmende vezels, die de input en output van bepaalde neuronen reguleren of remmen. Wat is beschreven als opioïde en serotonerge antagonisten, wordt verondersteld zowel lokale opiaat-analgesie als door hersenstimuli gegenereerde analgesie om te keren. De sensorische signalen of impulsen in het centrale zenuwstelsel worden uiteindelijk gecontroleerd door zowel stijgende als dalende remmende systemen, waarbij endogene opioïden of andere endogene stoffen, zoals serotonine, als remmende mediatoren worden gebruikt. Pijn is een complexe perceptie die ook kan worden beïnvloed door een aantal andere factoren, waaronder emotionele toestand.
Mechanismen van pijnmodulatie
Oplopend en aflopend pijnonderdrukkingsmechanisme
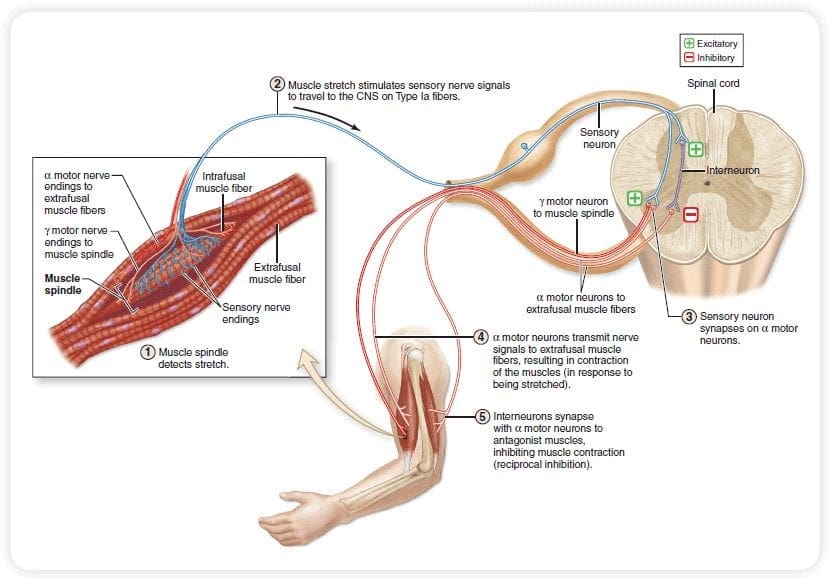
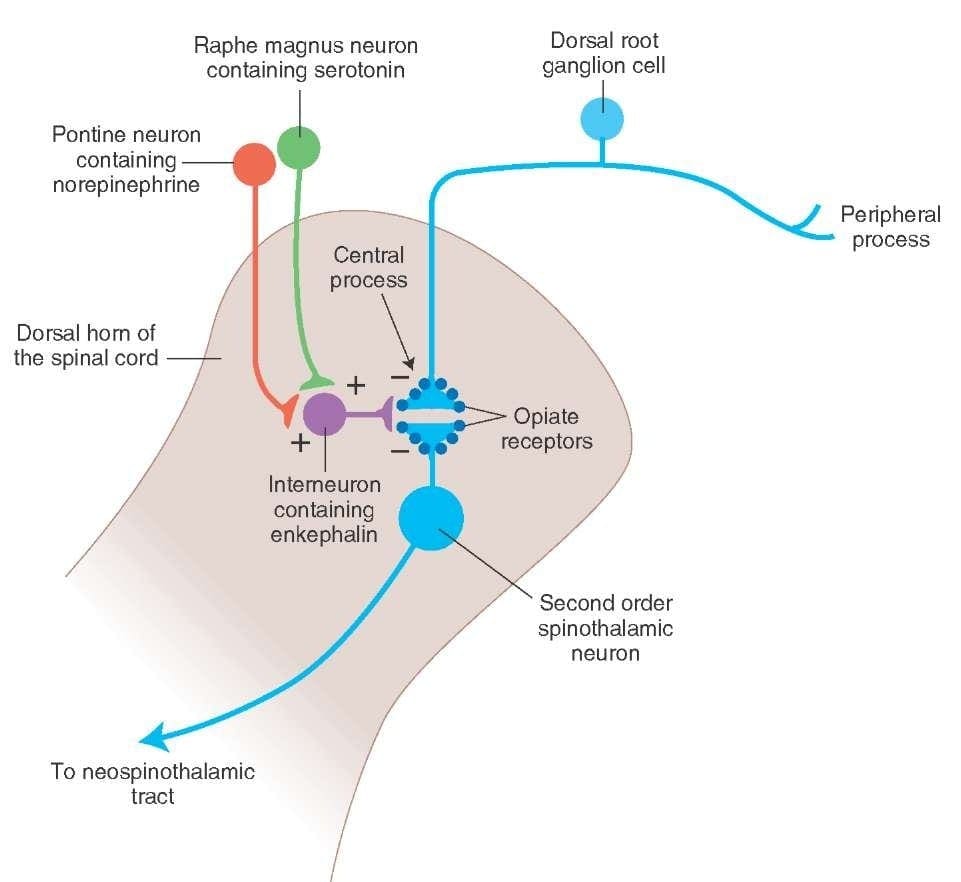
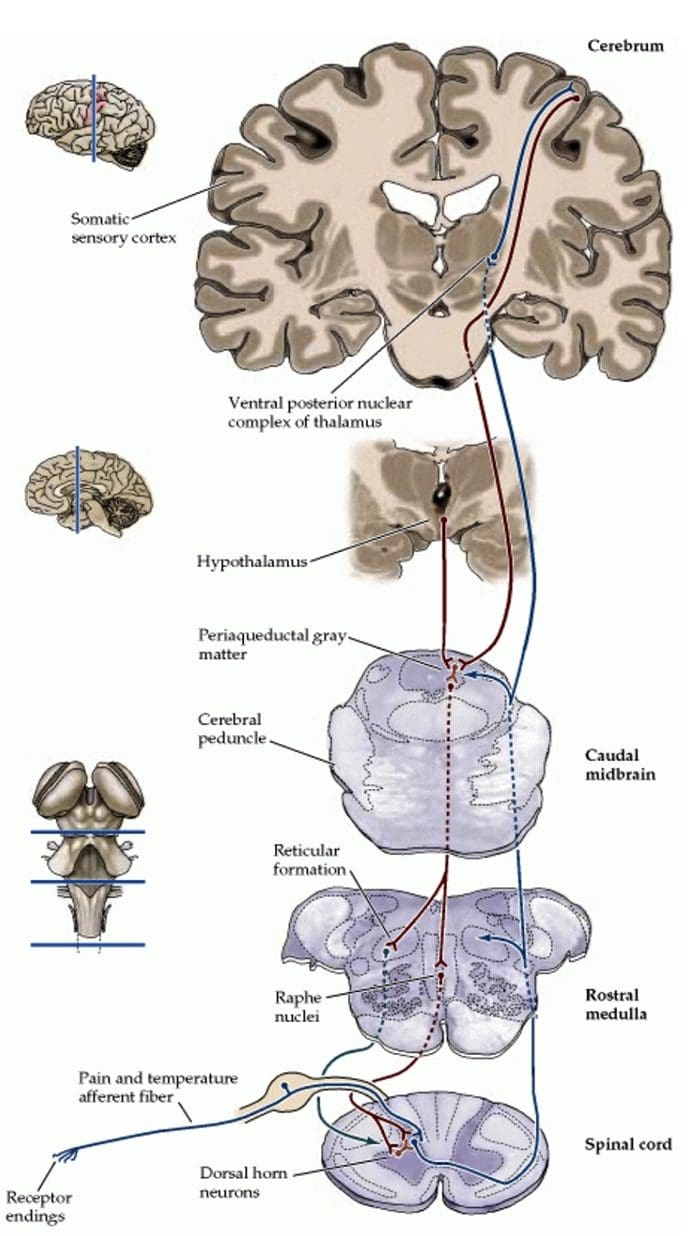
De primaire oplopende pijnvezels, zoals de A? en C-vezels bereiken de dorsale hoorn van het ruggenmerg vanuit perifere zenuwgebieden om de nociceptorneuronen in Rexed laminae I & II te innerveren. Cellen van Rexed lamina II maken synaptische verbindingen in Rexed-lagen IV tot VII. Cellen, met name binnen de laminae I en VII van de dorsale hoorn, geven aanleiding tot oplopende spinothalamische banen. Op het spinale niveau bevinden opiaatreceptoren zich in de presynaptische uiteinden van hun nocineuronen en in de interne niveaus IV tot VII van de dorsale hoorn.
Activering van opiaatreceptoren op het interneuronale niveau veroorzaakt hyperpolarisatie van de neuronen, wat leidt tot de remming van activering en de afgifte van substantie P, een neurotransmitter die betrokken is bij pijnoverdracht, waardoor pijnoverdracht wordt voorkomen. Het circuit dat bestaat uit de periaqueductale grijze of PAG-materie in de bovenste hersenstam, de locus coeruleus of LC, de nucleus raphe magnus of de NRM, en de nucleus reticularis gigantocellularis of Rgc, leidt tot de dalende pijn onderdrukkingspad, dat binnenkomende pijngegevens op ruggenmergniveau remt.
Zoals eerder vermeld, interageren opioïden met de opiaatreceptoren op verschillende niveaus van het centrale zenuwstelsel. Deze opiaatreceptoren zijn de normale doelgebieden voor hormonen en endogene opiaten, zoals de endorfines en enkefalines. Vanwege binding aan de receptor in subcorticale websites, secundaire veranderingen die resulteren in enige verandering in de elektrofysiologische eigenschappen van de neuronen en regulering van hun stijgende pijninformatie.
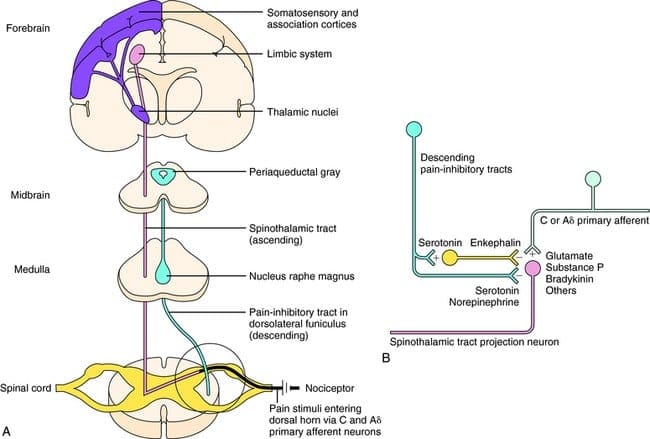
Wat activeert de PAG om zijn gevolgen uit te oefenen? Er werd ontdekt dat schadelijke stimulatie neuronen in de nucleus reticularis gigantocellularis of RGC triggert. De kern Rgc innerveert zowel PAG als NRM. De PAG stuurt axonen naar de NRM en zenuwen in de NRM sturen hun axonen naar het ruggenmerg. Bovendien blokkeren bilaterale dorsolaterale funiculus- of DLF-laesies, ook wel DLFX genoemd, de analgesie die wordt geproduceerd door zowel elektrische stimulatie als door micro-injectie van opiaten rechtstreeks in de PAG en NRM, maar ze verzwakken alleen de systemische analgetische effecten van opiaten. Deze waarnemingen ondersteunen de hypothese dat discrete dalende paden van de DLF nodig zijn voor zowel OA als SPA.
De DLF bestaat uit vezels die afkomstig zijn van verschillende hersenstamkernen, die serotonergisch kunnen zijn, of 5-HT, van zenuwen die zich in de nucleus raphe magnus of NRM bevinden; dopaminerge neuronen afkomstig van het ventrale tegmentale gebied, of VTA, en adrenerge neuronen afkomstig van de locus coeruleus, of LC. Deze dalende vezels onderdrukken schadelijke input in de nociceptieve neuronen van het ruggenmerg in laminae I, II en V.
Opiaatreceptoren zijn ook ontdekt in de dorsale hoorn van het ruggenmerg, voornamelijk in Rexed laminae I, II en V, en dergelijke spinale opiaatreceptoren bemiddelen remmende effecten op dorsale hoornneuronen die nociceptieve informatie doorgeven. De werking van morfine lijkt in gelijke mate te worden uitgeoefend in het ruggenmerg en de hersenstamkernen, inclusief de PAG en NRM. Systemische morfine werkt zowel op de opiaatreceptoren van de hersenstam als op de opiaatreceptoren van het ruggenmerg om analgesie te produceren. Morfine bindt de opiaatreceptoren van de hersenstam, die de serotonerge route van de hersenstam in het ruggenmerg en de DLF triggeren, en deze hebben een opioïde-gemedieerde synaps op het niveau van het ruggenmerg.
Deze observatie toont aan dat schadelijke stimuli, in plaats van niet-schadelijke stimulus, de poortcontroletheorie bepalen, die cruciaal is voor de activering van het dalende pijnmodulatiecircuit waar pijn pijn remt via de dalende DLF-route. Daarnaast zijn er opgaande verbindingen in de PAG en de raphe-kernen in het PF-CM-complex. Deze thalamische regio's maken deel uit van de stijgende pijnmodulatie op de diencephalon-graad.
Stress-geïnduceerde analgesie (SIA)
Analgesie kan worden geproduceerd in bepaalde stressvolle omstandigheden. Blootstelling aan veel verschillende stressvolle of pijnlijke gebeurtenissen genereert een pijnstillende reactie. Dit fenomeen staat bekend als stress-geïnduceerde analgesie of SIA. Aangenomen wordt dat stress-geïnduceerde analgesie inzicht geeft in de fysiologische en psychologische factoren die endogene pijnbeheersing en opiaatsystemen veroorzaken. Bijvoorbeeld, soldaten die gewond zijn geraakt in de strijd of sporters die gewond zijn geraakt tijdens het sporten, melden soms dat ze geen pijn of ongemak voelen tijdens het gevecht of spel, maar ze zullen de pijn achteraf doorstaan als de specifieke situatie is gestopt. Bij dieren is aangetoond dat elektrische schokken door stress veroorzaakte analgesie veroorzaken. Op basis van deze experimenten wordt aangenomen dat de druk die de soldaten en atleten ervoeren, de pijn onderdrukte die ze later zouden ervaren.
Er wordt aangenomen dat endogene opiaten worden geproduceerd als reactie op stress en pijn remmen door het neerwaartse systeem van de middenhersenen te activeren. Bovendien vertoonden sommige SIA kruistolerantie met opiaat-analgesie, wat aangeeft dat deze SIA wordt gemedieerd via opiaatreceptoren. Experimenten die verschillende parameters van elektrische schokstimulatie gebruiken, tonen dergelijke door stress veroorzaakte analgesie aan en sommige van die angsten die analgesie veroorzaken, kunnen worden geblokkeerd door de opioïde-antagonist naloxon, terwijl andere niet worden geblokkeerd door naloxon. Samenvattend leiden deze observaties tot de beslissing dat er zowel opiaat- als niet-opiaatvormen van SIA bestaan.
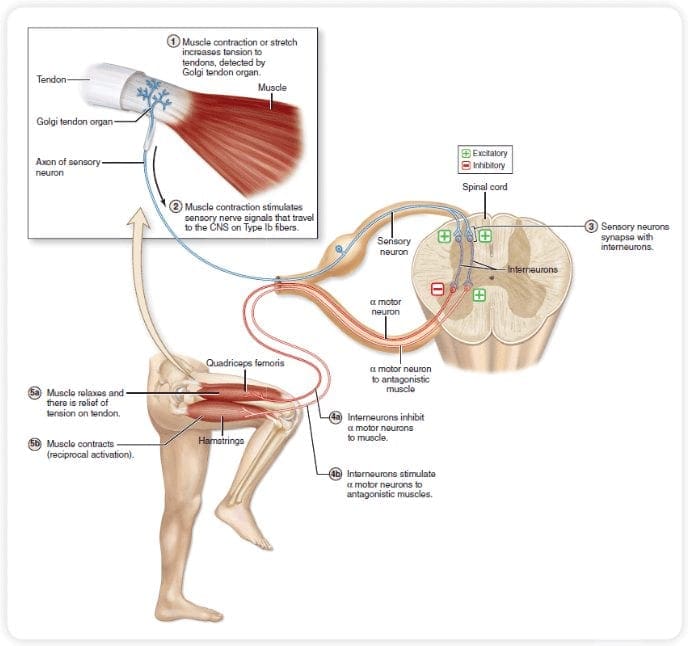
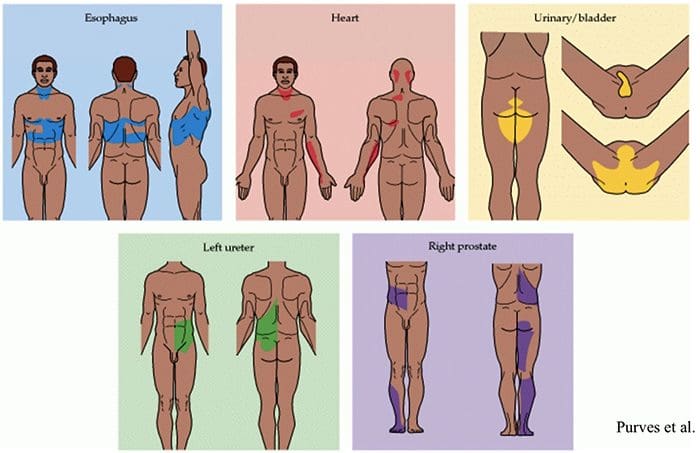
Somatoviscerale reflex
De somatoviscerale reflex is een reflex waarbij viscerale functies worden geactiveerd of geremd door somatische sensorische stimulatie. Bij proefdieren is bewezen dat zowel schadelijke als onschadelijke stimulatie van somatische afferenten reflexveranderingen opwekt in sympathische efferente activiteit en, bijgevolg, effector-orgaanfunctie. Deze verschijnselen zijn aangetoond in gebieden als het maagdarmkanaal, de urinewegen, de bijniermerg, lymfatische cellen, het hart en de bloedvaten van de hersenen en de perifere zenuwen.
Meestal worden incisies experimenteel uitgelokt door stimulatie van huidafferenten, hoewel er ook enig werk is gedaan aan spier- en gewrichtsafferenten, inclusief die van ruggenmergcellen. De uiteindelijke reacties vertegenwoordigen de integratie van meerdere tonische en reflexinvloeden en kunnen lateraliteit en segmentale trends vertonen, evenals variabele prikkelbaarheid in overeenstemming met de betrokken afferenten. Gezien de complexiteit en veelheid van mechanismen die betrokken zijn bij de laatste expressie van de reflexrespons, moeten pogingen om te extrapoleren naar klinische situaties hoogstwaarschijnlijk worden uitgevoerd ten gunste van verder systematisch fysiologisch onderzoek.
De reikwijdte van onze informatie is beperkt tot zowel chiropractie als verwondingen en aandoeningen van de wervelkolom. Om het onderwerp te bespreken, aarzel dan niet om Dr. Jimenez te vragen of contact met ons op te nemen 915-850-0900 .
Curator van Dr. Alex Jimenez
Bijkomende onderwerpen: Sciatica
Ischias wordt medisch een verzameling symptomen genoemd, in plaats van één enkele verwonding en / of aandoening. Symptomen van heupzenuwpijn, of ischias, kunnen variëren in frequentie en intensiteit, maar het wordt meestal beschreven als een plotselinge, scherpe (mesachtige) of elektrische pijn die vanaf de lage rug langs de billen, heupen, dijen en benen in de voet. Andere symptomen van ischias kunnen zijn: tintelingen of branderige gevoelens, gevoelloosheid en zwakte langs de lengte van de heupzenuw. Ischias treft meestal individuen tussen de leeftijden van 30 en 50 jaar. Het kan zich vaak ontwikkelen als gevolg van de degeneratie van de wervelkolom als gevolg van ouderdom, maar de compressie en irritatie van de nervus ischiadicus veroorzaakt door een uitstulping of herniated disc, onder andere spinale gezondheidsproblemen, kan ook heupzenuwpijn veroorzaken.

EXTRA BELANGRIJK ONDERWERP: Chiropractor Ischias Symptomen



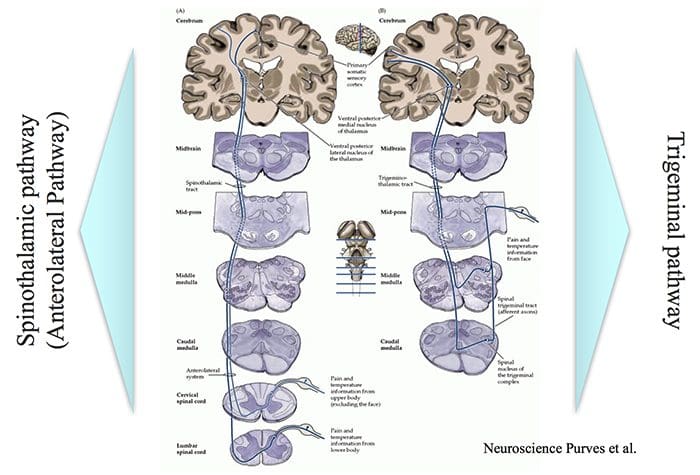
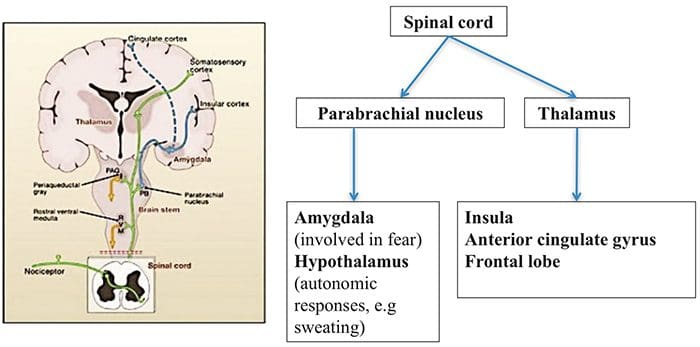 Hersengebieden die betrokken zijn bij de verwerking van nociceptieve signalen
Hersengebieden die betrokken zijn bij de verwerking van nociceptieve signalen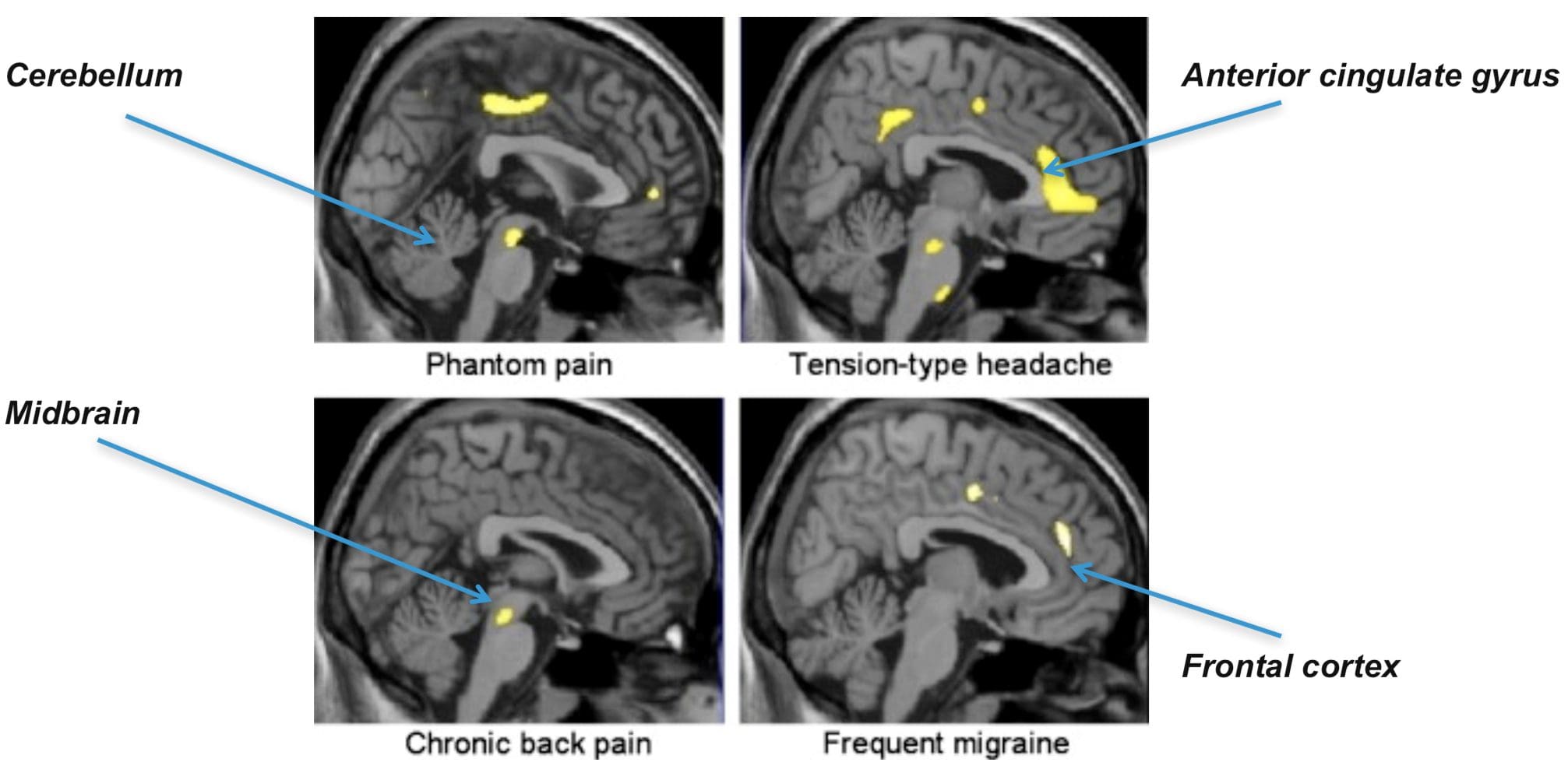 Het anterior cingulate en de insula cortex worden geactiveerd bij mensen
Het anterior cingulate en de insula cortex worden geactiveerd bij mensen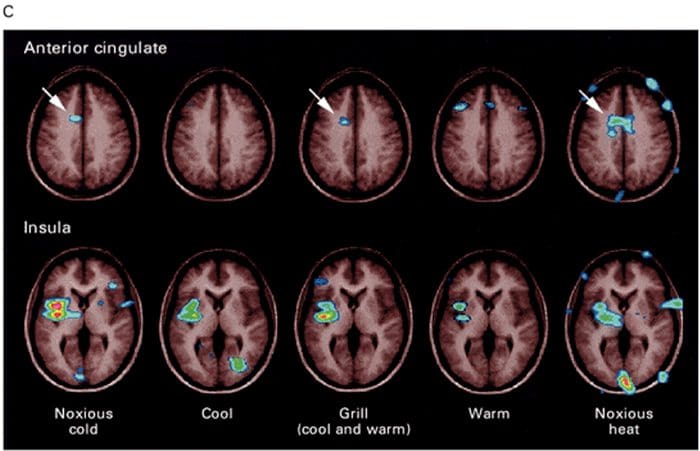
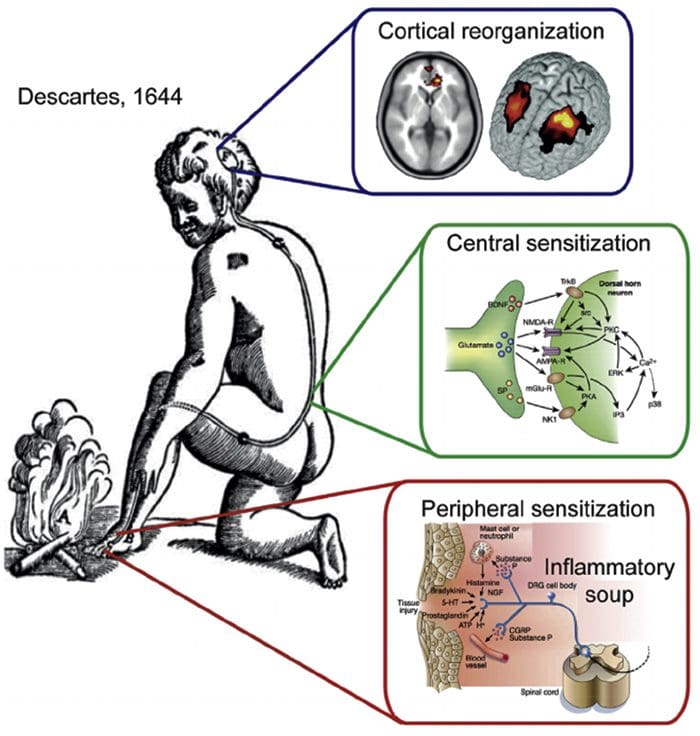
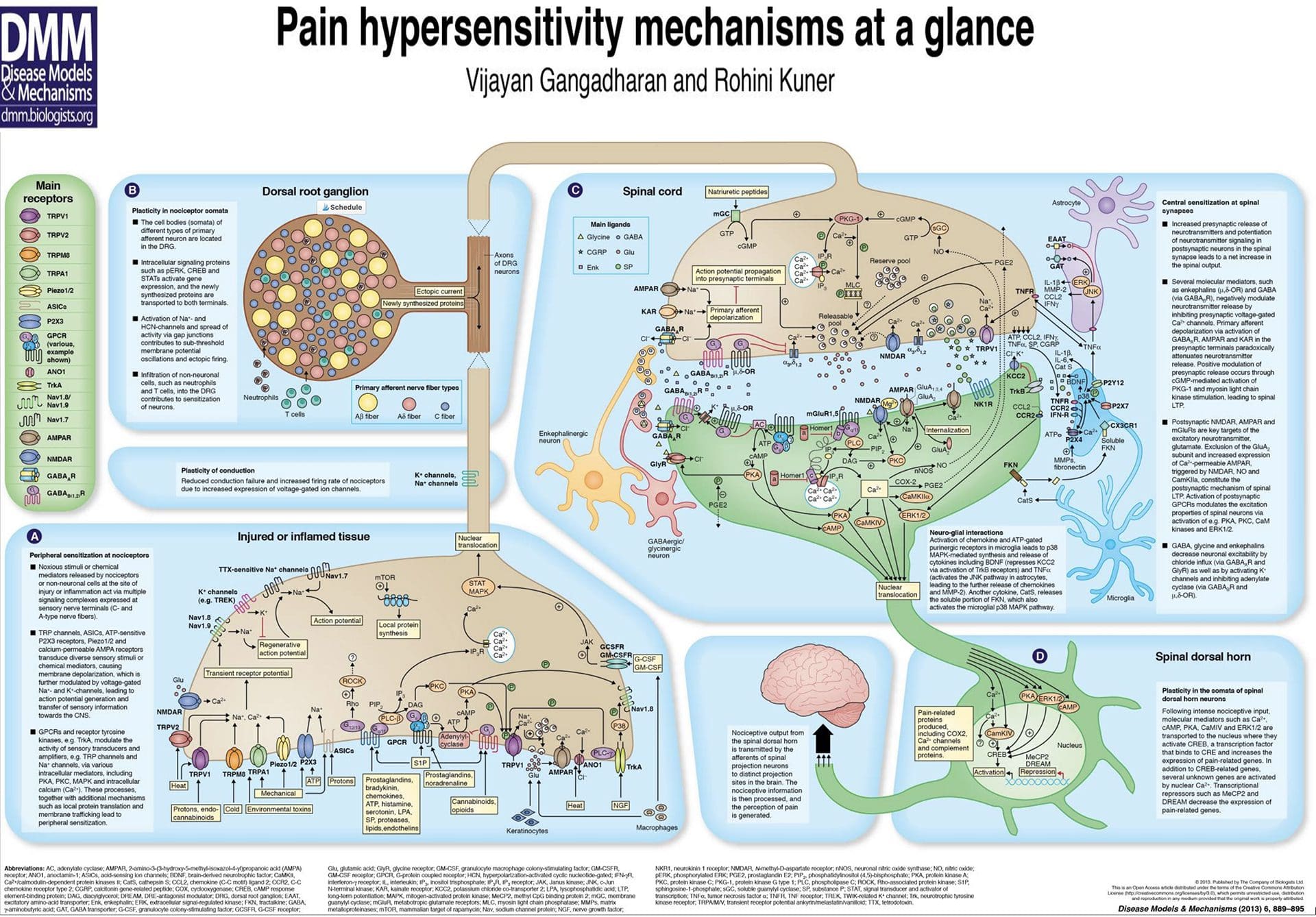
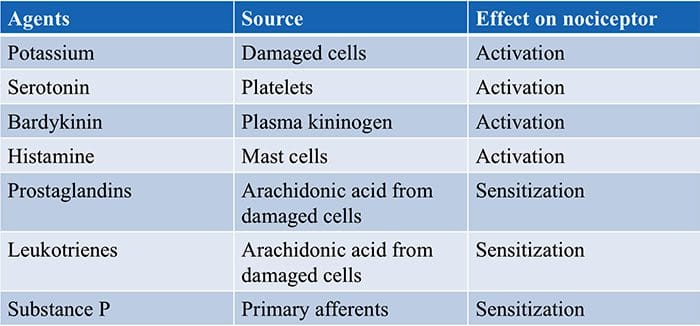
 Ontstekingssoep – Hyperalgesie
Ontstekingssoep – Hyperalgesie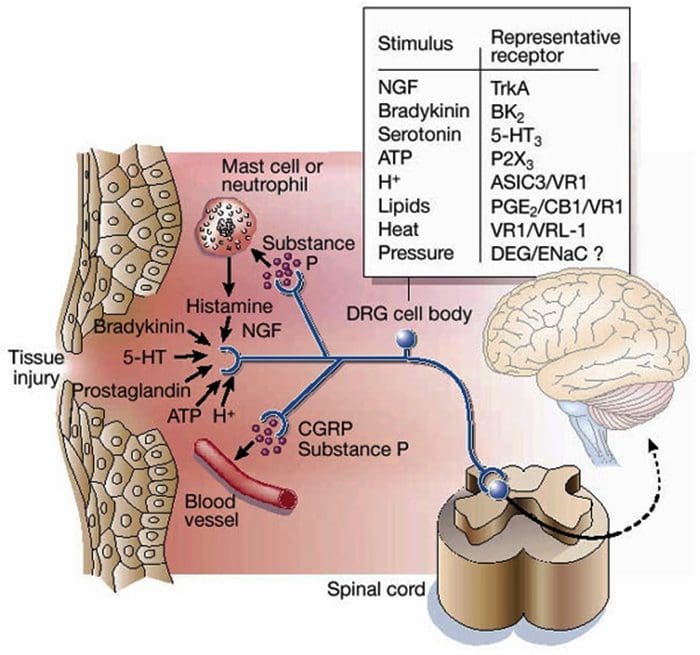
 Gate Control Theorie van pijn
Gate Control Theorie van pijn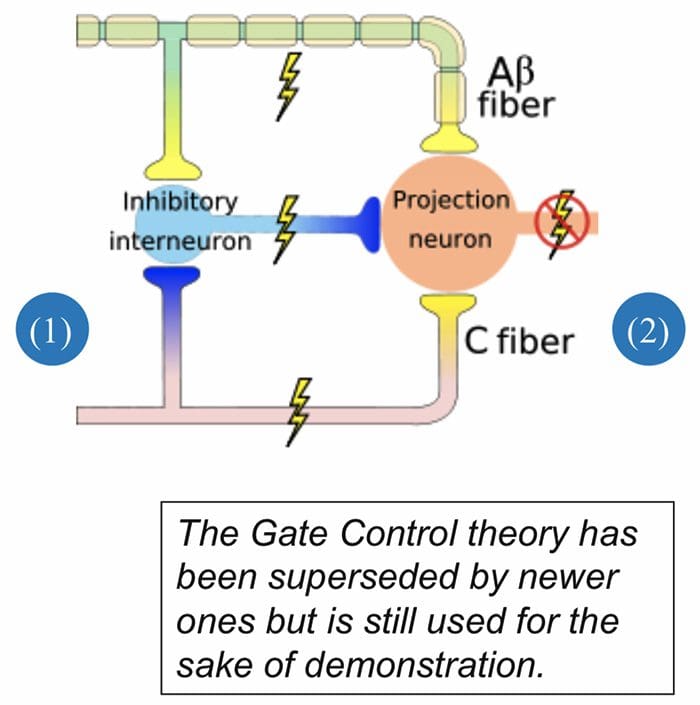
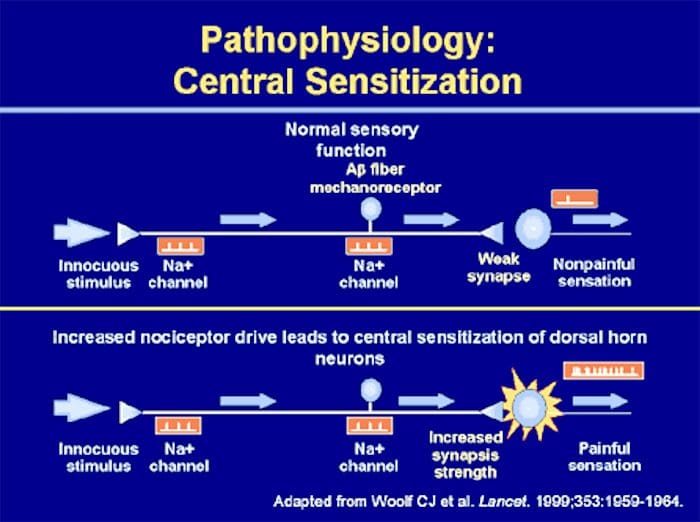
 Afwijkingen van het pijnsysteem
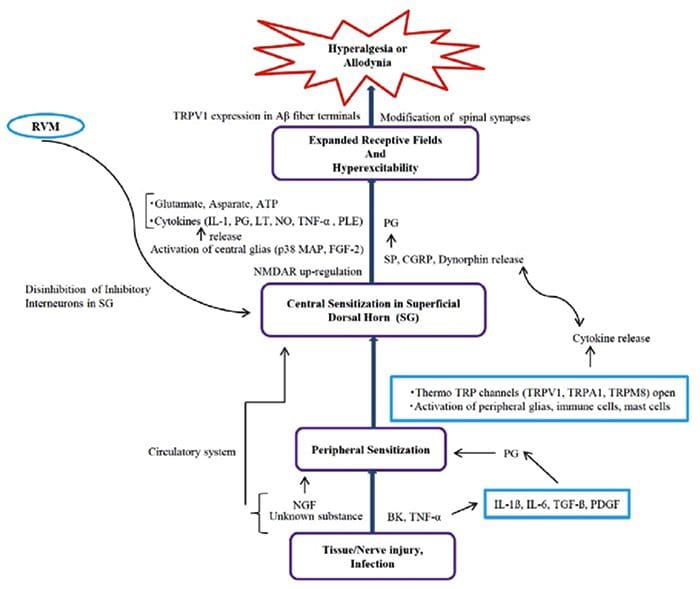
Afwijkingen van het pijnsysteem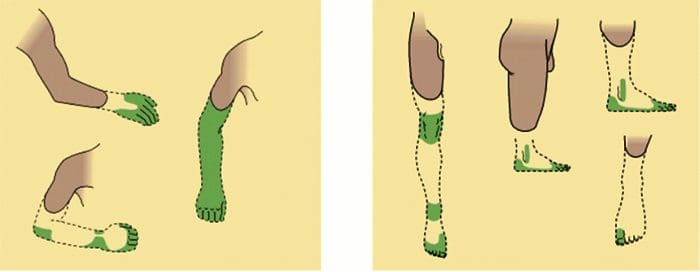 Perifere sensibilisatie
Perifere sensibilisatie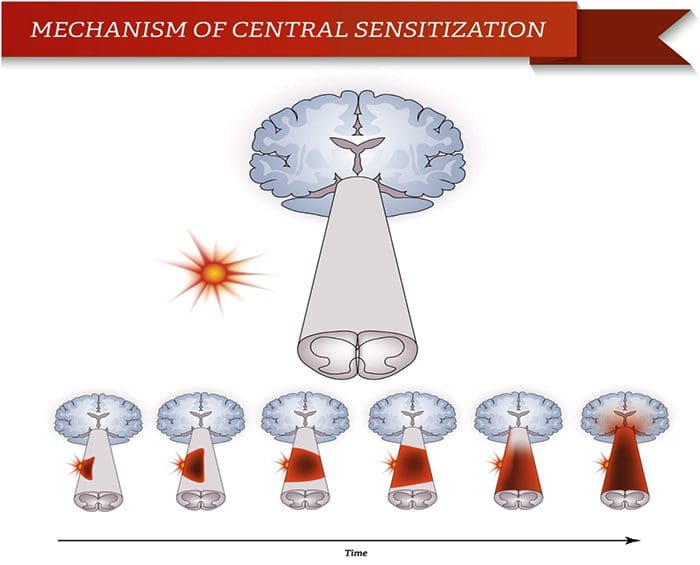
 Somatosensorische Cortex-organisatie
Somatosensorische Cortex-organisatie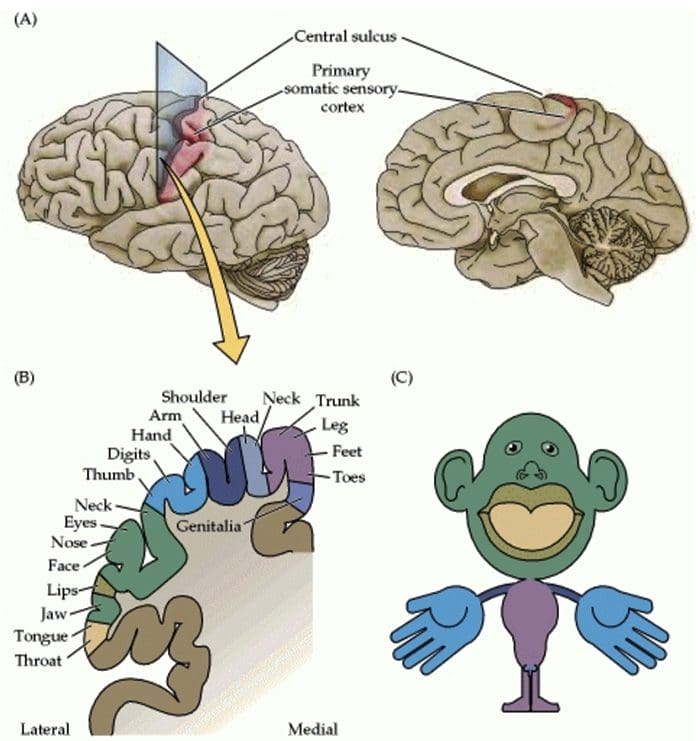 Corticale reorganisatie
Corticale reorganisatie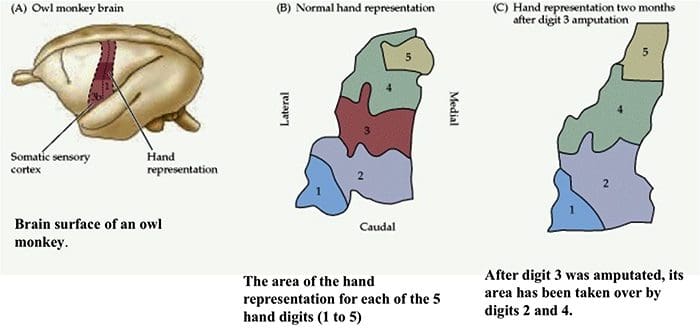

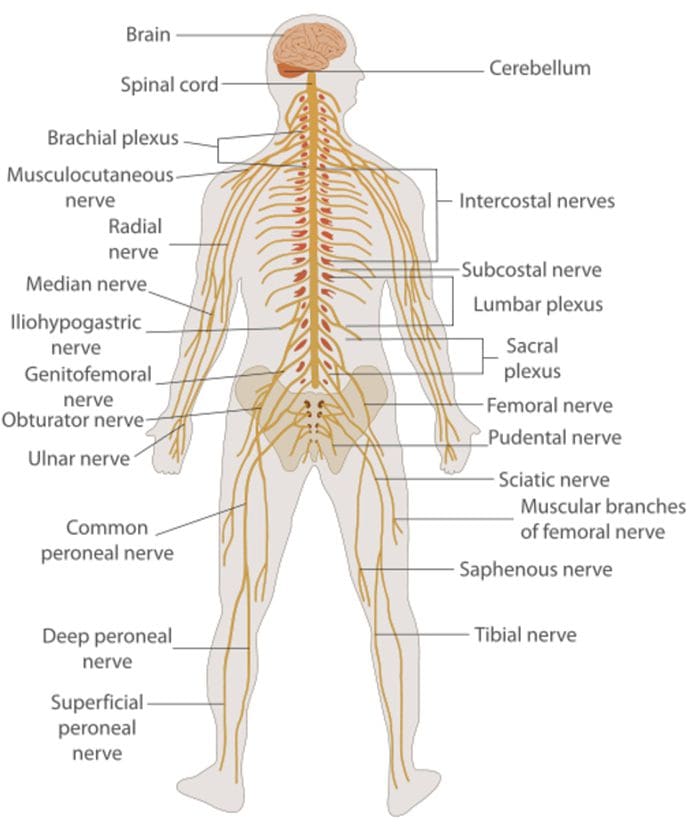
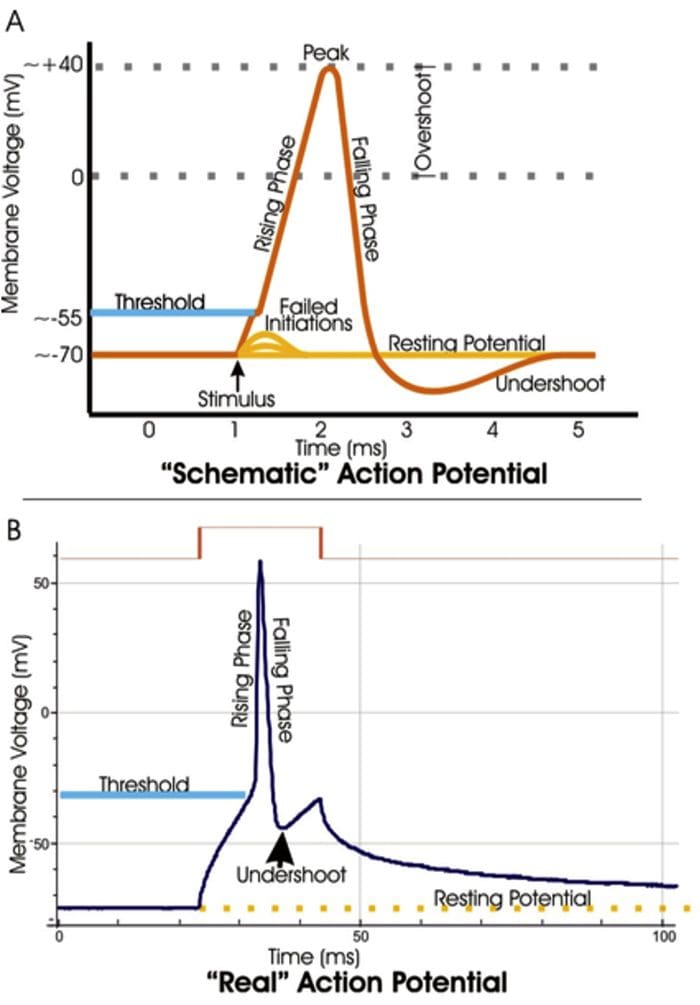
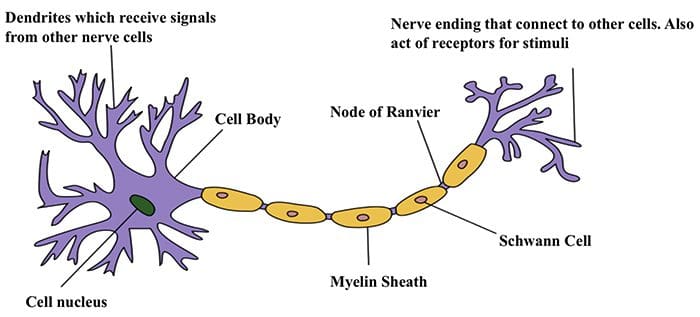 Zenuwcel-naar-zenuwcel communicatie
Zenuwcel-naar-zenuwcel communicatie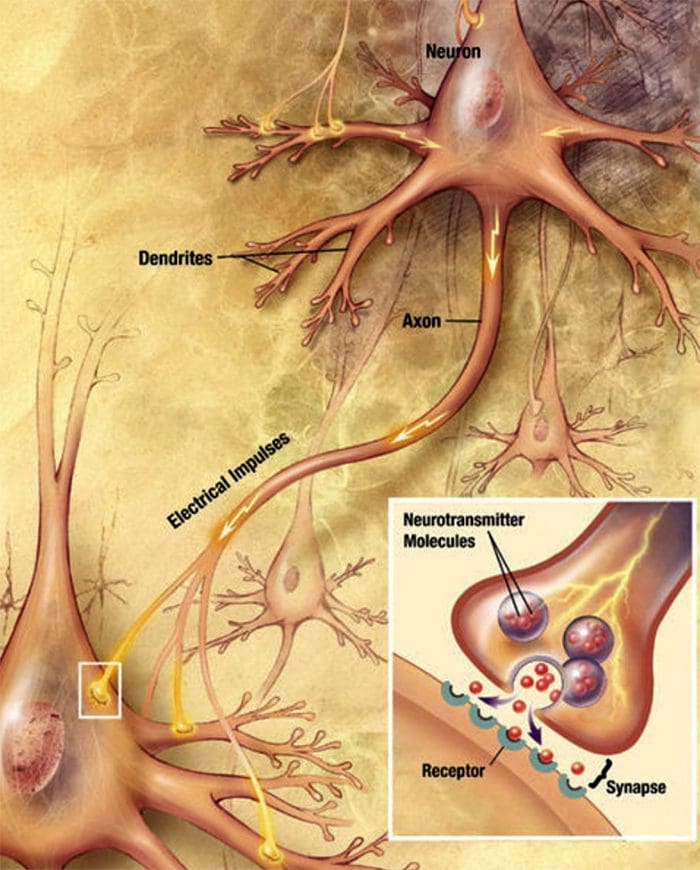 Zenuwcellen communiceren met andere cellen door een chemische stof af te geven uit de zenuwuiteinden Neurotransmitters
Zenuwcellen communiceren met andere cellen door een chemische stof af te geven uit de zenuwuiteinden Neurotransmitters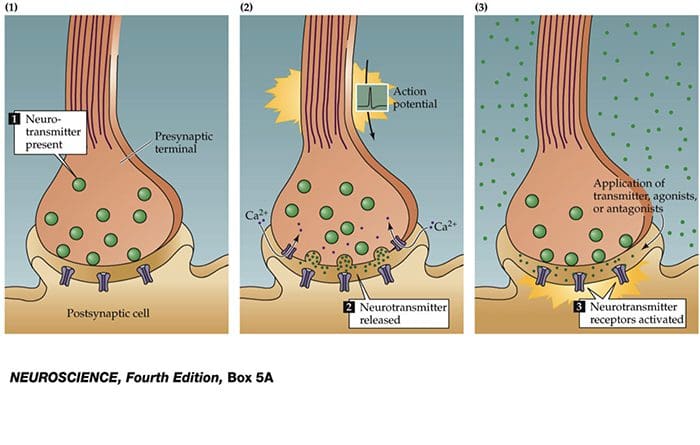
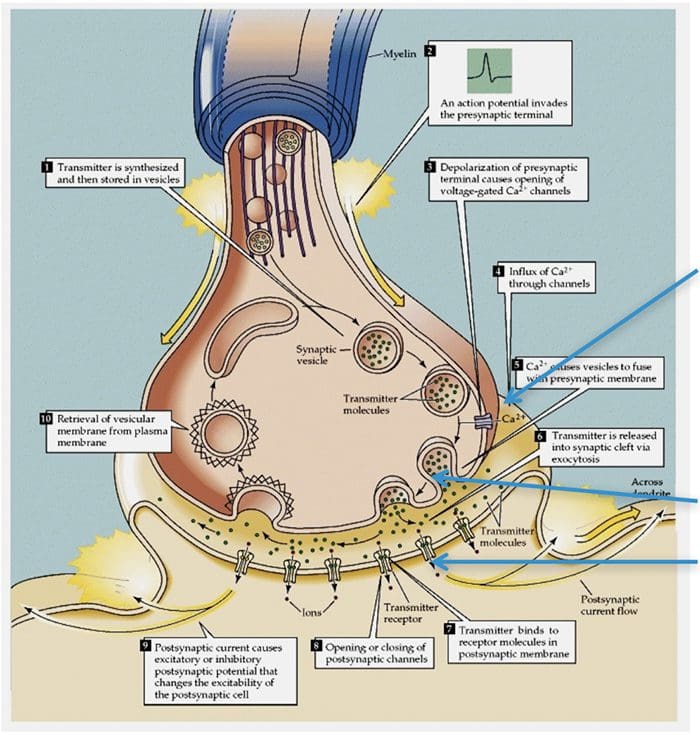
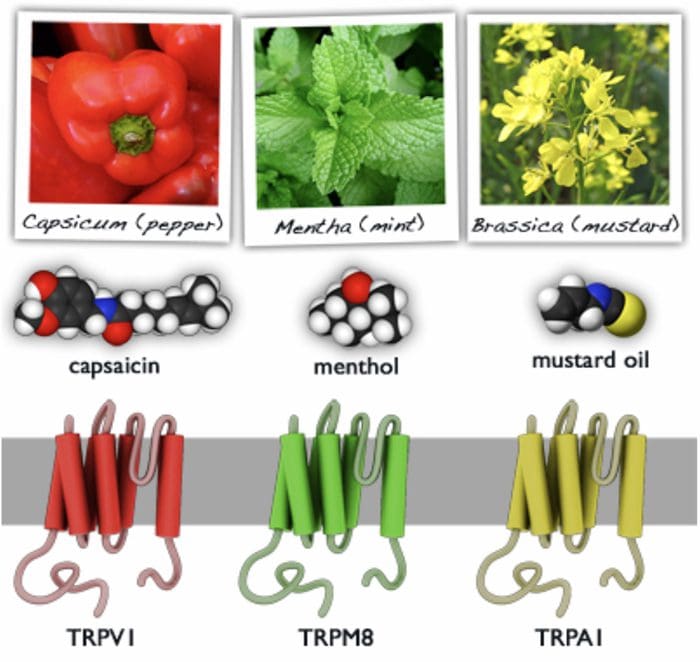
 TRP-kanalen
TRP-kanalen